Большинство фармакологических эффектов антидепрессантов обусловлено их влиянием на уровень межнейронной передачи импульсов.
Ингибиторы МАО блокируют метаболические пути разрушения нейромедиаторов (норадреналина, серотонина, дофамина), а трициклические антидепрессанты - их обратный захват пресинаптической мембраной, что приводит к повышению содержания свободных нейромедиаторов в синаптической щели. Это обуславливает повышение продолжительности и интенсивности их воздействия на постсинаптическую мембрану. Механизм обратного захвата в норме предотвращает гиперстимуляцию рецепторов постсинаптической мембраны.
Установлено, что вторичные амины преимущественно блокируют обратный захват норадреналина, а третичные амины - как норадреналина, так и серотонина (кломипрамин даже в большей степени блокирует обратный захват серотонина).
Потенцирование серотонинергических структур мозга связывается с основным тимоаналептическим действием антидепрессантов, а норадренергических - с общим активирующим, в том числе психо-
моторную сферу, действием. Установлено, что норадреналин является нейромедиатором, поддерживающим уровень бодрствования и принимающим участие в формировании когнитивных адаптационных реакций, а серотонин осуществляет контроль за импульсивными влечениями, половым поведением, снижением агрессивности, аппетита, облегчением засыпания, регуляцией циклов сна, уменьшением чувствительности к боли, поэтому его называют нейромедиатором «хорошего самочувствия».
Экспериментальным путём была определена активность блокады обратного захвата норадренална и серотонина. Установлены большие различия в проявлении этого эффекта: так, мапротилин в 470 раз активнее блокирует обратный захват норадреналина, чем серотонина; дезипрамин - в 380 раз, доксепин - в 15 раз, а классические трициклические антидепрессанты - имипрамин и амитриптилин - соответственно только в 3,2 и в 2,8 раза. Тразодон, напротив, в 26 раз, а кломипрамин в 5 раз сильнее блокируют обратный захват серотонина, чем норадреналина (см. табл. 28-9).
В настоящее время выделяется особая группа антидепрессантов, так называемая группа ингибиторов обратного захвата серотонина, с еще большей избирательностью блокирующего действия на обратный захват серотонина. К ним относятся флувоксамин, флуоксетин, циталорам, сертралин и пароксетин.
Таблица 28-24. Сравнительная активность некоторых антидепрессантов по способности блокировать обратный захват норадреналина по отношению к серотонину
 При оценке спектра фармакологической активности антидепрессанта нужно иметь в виду, что избирательность действия не равнозначна силе блокирующего влияния на обратный захват нейромедиатора. Так, по этому показателю наиболее активным воздействием на обратный захват норадреналина в экспериментальных условиях обладает дезипрамин (см. табл. 28-10), который почти в 4 раза превосходит идущие вслед за ним нортриптилин, амоксапин и мапротилин. Существенную активность в этом отношении имеют также имипрамин, доксепин, амитриптилин, кломипрамин. Остальные препараты достаточно слабо блокируют обратный захват норадреналина.
При оценке спектра фармакологической активности антидепрессанта нужно иметь в виду, что избирательность действия не равнозначна силе блокирующего влияния на обратный захват нейромедиатора. Так, по этому показателю наиболее активным воздействием на обратный захват норадреналина в экспериментальных условиях обладает дезипрамин (см. табл. 28-10), который почти в 4 раза превосходит идущие вслед за ним нортриптилин, амоксапин и мапротилин. Существенную активность в этом отношении имеют также имипрамин, доксепин, амитриптилин, кломипрамин. Остальные препараты достаточно слабо блокируют обратный захват норадреналина.
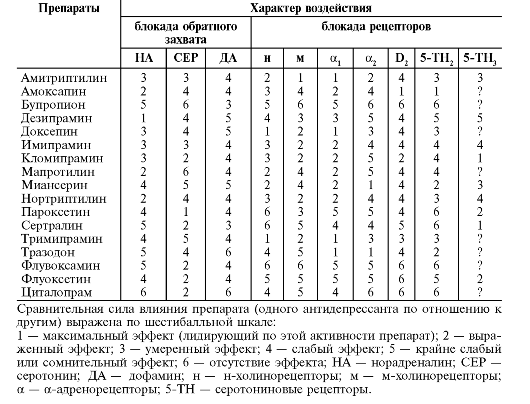
Таблица 28-25. Сравнительная фармакологическая активность антидепрессантов
 По выраженности блокирующего влияния на обратный захват серотонина выделяются пароксетин, сертралин и кломипрамин, причём последний в 2 раза превосходит известный серотонинергический антидепрессант флувоксамин и в 4 раза - флуоксетин, за которым следуют амитриптилин и имипрамин. При этом амитриптилин действует в 3 раза активнее тразодона, который является высоко избирательным,
По выраженности блокирующего влияния на обратный захват серотонина выделяются пароксетин, сертралин и кломипрамин, причём последний в 2 раза превосходит известный серотонинергический антидепрессант флувоксамин и в 4 раза - флуоксетин, за которым следуют амитриптилин и имипрамин. При этом амитриптилин действует в 3 раза активнее тразодона, который является высоко избирательным,
но слабым блокатором обратного захвата серотонина. За ним идёт основная группа антидепрессантов.
Из таблиц также следует, что наиболее активными антидепрессантами, неизбирательно блокирующими как обратный захват серотонина, так и норадреналина, является классическая триада трициклических антидепрессантов (имипрамин, амитриптилин и кломипрамин), эффективность которых при депрессиях проверена многолетним опытом их практического применения. Среди них следует выделить кломипрамин, который, наряду с равным по активности двум другим препаратам норадренергическим действием, в 5 раз сильнее блокирует пресинаптический захват серотонина и является одним из самых активных тимоаналептических средств.
Выяснилось также, что молекулы антидепрессантов, в частности нефазодона, способны непосредственно блокировать рецепторы постсинаптической мембраны, препятствуя действию нейромедиаторов. Прямое воздействие препаратов на постсинаптическую мембрану в настоящее время признается важной составной частью их антидепрессивного эффекта.
Кроме того, синтезированы и введены в практику препараты «двойного» действия, ингибирующие обратный захват как серотонина, так и норадреналина - милнаципран, миртазапин и др. Миртазапин по механизму обратной связи блокирует α2-рецепторы или ауторецепторы и, таким образом, способствует выбросу серотонина и норадреналина в синаптическую щель, с одной стороны. С другой стороны, он блокирует 5НТ2- и 5НТ3-рецепторы и серотонину приходится связываться с 5НТ1-рецепторами, с которыми и связано развитие собственно тимоаналептического эффекта.
Существуют также препараты, обнаруживающие отчётливые тимоаналептические свойства, механизм действия которых остаётся до конца не понятным. К этим препаратам относятся тианептин (коаксил), S-аденозинметионин (гептрал), некоторые бензодиазепиновые производные, например, алпразолам и нейропептиды. В частности, тианептин усиливает обратный захват серотонина пресинаптической мембраны, т.е. фактически оказывает действие, противоположное эффектам основных антидепрессантов, и способствует усилению сберегающего естественного механизма этого нейромедиатора в пресинаптическом окончании. Кроме того, препарат путём геномрегуляторных механизмов способствует уменьшению количества или плотности серотониновых рецепторов на постсинаптической мембране, что ведёт к снижению чувствительности постсинаптической мембраны к серотонину и тем самым обеспечивает тианептину более высокую переносимость. Было показано, что тианептин способен коррегировать стрессовый
выброс адреналина через гипоталамо-гипофизарно-надпочечниковую систему, а также тианептин имеет нейропротективные свойства, так как способен увеличивать длину и число апикальных дендритов пирамидальных клеток гиппокампа. Еще одним достоинством тианептина является его способность увеличивать содержание внеклеточного дофамина во фронтальной коре, а этот механизм, свойственный атипичным нейролептикам, принято связывать с редуцирующим воздействием на дефицитарную симптоматику шизофрении, в частности на когнитивные дисфункции.
Антидепрессанты связываются с различными рецепторами как в центральной, так и в периферической нервной системе. Однако их воздействие по сравнению с более специфическими средствами, используемыми в соматической медицине, относительно невелико.
Многие препараты клинически значимо блокируют м-холинорецепторы и Н1-гистаминовые рецепторы. В последние годы получены данные, что некоторые трициклические антидепрессанты (амитриптилин, имипрамин, кломипрамин, дезипрамин) могут связываться также с опиатными рецепторами, чем, вероятно, объясняются их антиноцептивные (аналгезирующие) свойства.
Важная роль в механизмах развития эффекта антидепрессанта принадлежит изменению в процессе терапии рецепторной чувствительности. Этим, в частности, объясняется отставленность на 2- 3 нед их клинического эффекта. Практически все антидепрессанты в эксперименте после трёхнедельного введения вызывают уменьшение числа постсинаптических β-адренорецепторов, снижают выработку циклического цАМФ. Трициклические антидепрессанты вызывают гиперчувствительность α1-адренорецепторов (увеличение плотности) и снижают чувствительность (уменьшение плотности и функциональной активности) β-адрено-, ГАМК- (типа Б), α2-адрено- и серотониновых рецепторов (типа 5ТН2) на постсинаптической мембране в кортикальных структурах мозга, а также снижают функциональную активность дофаминовых ауторецепторов, увеличивают плотность, но снижают активность лимбических серотониновых (типа 5ТН1а) рецепторов. Таким образом, можно отметить, что тимоаналептический эффект любого антидепрессанта, особенно при длительном применении, реализуется посредством комплексного воздействия на большинство нейромедиаторных и рецепторных систем мозга. Эти эффекты могут быть объяснены в свете взаимодействия между различными моноаминергическими системами мозга. Стимуляция одной системы приводит к быстрым или отставленным по времени изменениям в другой системе моноаминов. Поэтому индивидуальный спектр эффектов антидепрессанта зависит от соотношения первичности и выраженности
этих воздействий. Взаимосвязь фармакологических эффектов антидепрессантов с их клиническими проявлениями представлена в табл.
28-26.
Таблица 26. Фармакологические свойства антидепрессантов и их клинические проявления
 Продолжение табл. 28-26
Продолжение табл. 28-26
 Окончание табл. 28-26
Окончание табл. 28-26
 Фармакокинетика
Фармакокинетика
При пероральном приёме трициклические антидепрессанты быстро всасываются и распределяются по всему организму. Около 50% введённой дозы элиминируется в среднем за двое суток, преимущественно с мочой, остальная часть связывается с белками крови и полностью утилизируется лишь через 2 нед.
Большинство как трициклических, так и серотонинергических антидепрессантов метаболизируется путём гидроксилирования ферментами печени, изоферментом цитохрома CYP2D6, активность которого может индивидуально варьировать вследствие генетического полиморфизма, чем отчасти определяется и эффективность терапии (см. главу 7 «Клиническая фармакогенетика»).
Многие метаболиты активны и играют роль большую, чем основной препарат в формировании терапевтического эффекта.
Норфлуоксетин по сравнению с флуоксетином имеет существенно больший период полувыведения, что во многом определяет характер побочных реакций последнего.
N-дезметилциталопрам значительно активнее действует, по сравнению с норфлуоксетином в отношении блокады обратного захвата норадреналина.
Для некоторых трициклических антидепрессантов (нортриптилин и бупропион) имеется «терапевтическое окно» концентрации, при которых развивается клинический эффект. Многие трициклические
антидепрессанты имеют линейную зависимость между их содержанием в плазме крови и клинической эффективностью. Так, например, при концентрации имипрамина в плазме крови меньше 150 нг/мл клинический эффект отмечался только у 29% больных, а при концентрации больше 250 нг/мл - у 93% больных. Следовательно, у таких препаратов дозу можно повышать до уровня переносимой или до наступления эффекта. Однако для большинства антидепрессантов, в том числе последнего поколения, чёткой связи между эффектом и концентрацией в крови не найдено. Более того, оказалось, что серотонинергические антидепрессанты, независимо от концентрации в крови, часто оказываются более эффективными при применении в низких дозах.
Период полувыведения широко варьирует у отдельных антидепрессантов и составляет, например, для имипрамина и флувоксамина - 15 ч, для амитритилина - 16 ч, для пароксетина - 20 ч, для нортриптилина - 24 ч, для сертралина - 25 ч, а для протриптилина - 126 ч, флуоксетина - около 60 ч, а его метаболита (норфлуоксетина) около 300 ч (7-15 дней!) (табл. 28-12). У препаратов с длительным периодом полувыведения равновесная концентрация достигается значительно позднее (у флуоксетина, например, через 1-4 мес после начала лечения), но реже возникает синдром отмены при резком прекращении приёма препарата.
Скорость выведения из организма является важной характеристикой антидепрессантов, по крайней мере, исходя из двух соображений: во-первых, - частоты назначения препарата и, во-вторых, - риска развития тяжёлой интоксикации при передозировке препаратов с длительным периодом полувыведения. Депрессивные больные, как известно, достаточно часто используют «подручные» ЛС в суицидальных целях.
Содержание антидепрессанта в плазме крови у отдельных больных может различаться в 5-10 раз. Такой разброс связан, главным образом, с индивидуальными различиями процессов метаболизма в печени. Их скорость зависит от многих причин: генетически детерминированной активности цитохромов CYP, функционального состояния печени и организма в целом, явлений лекарственной аутоиндукции или аутоингибирования ферментов (например, повышенные дозы флуоксетина и пароксетина угнетают метаболическую активность изофермента цитохрома CYP2D6, что может приводить к существенному увеличению их содержания в крови и удлинению периода полувыведения), от применяемого препарата (например, превращение имипрамина в дезипрамин происходит значительно быстрее, чем амитриптилина в
нортриптилин) и во многом также от возраста больного. Пожилые вследствие замедленного метаболизма склонны к быстрому развитию тяжёлых побочных эффектов, особенно при применении третичных аминов, которые уменьшают и без того сниженную окислительную активность ферментов печени. У детей метаболизм, наоборот, ускорен и в пересчёте на единицу массы тела иногда требуется применение более высоких доз препарата, хотя именно в этом возрасте передозировка антидепрессантов особенно опасна. Кроме того, уровень антидепрессанта в плазме крови может существенно изменяться вследствие различных лекарственных взаимодействий.
Показания
Депрессии различного генеза, в том числе депрессивные состояния циклотимического уровня, дистимии, меланхолический синдром, атипичные депрессии, астенические и адинамические расстройства, депрессии с идеаторной и двигательной заторможенностью, деперссивные нарушения с ипохондрической симптоматикой и др. Паническое расстройство, обсессивно-компульсивное расстройство, социальная фобия, нервная анорексия и булимия, нарколепсия, соматоформные расстройства. В клинике алкоголизма их применяют вне периода абстиненции, при повышенной утомляемости, при отсутствии выраженной тревоги, бессоннице, дисфорических нарушениях.
Противопоказания
Состояние возбуждения, судорожные припадки, острые случаи спутанности сознания, поражения печени и почек в стадии декомпенсации, стойкая гипотензия, нарушение кровообращения. Беременность. Индивидуальная непереносимость.