Сходства и различия в строении белков и нуклеиновых кислот
БЕЛКИ.
Имеют полимерное строение (сложные полимеры, или поликонденсаты), состоят из множества мономеров. Мономерам белка являются различные аминокислоты (NH2-CHR-COOH). 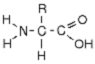
В составе любой аминокислоты к одному и тому же атому углерода присоединяются две сильно заряженные группы (аминогруппа NH2+ и карбоксильная группа COOH-), благодаря своим свойствам аминокислоты могут принимать участие в сложных химических реакциях, в т.ч. в образовании длинных полимеров. Белки — главный функциональный элемент любого организма. У всех живых существ в формировании белков принимают участие 20 основных аминокислот. Средний размер белка — около 300 аминокислот. Функция конкретного белка определяется последовательностью его аминокислот.
Радикалы:
1 – не несут на себе заряда совсем (углеводородные остатки)
2 – радикалы со слабыми электростатическими зарядами (гидроксильная, карбонильная, тиогруппы)
3 – имеющие сильный положительный заряд (аминогруппа)
4 – сильный отрицательный заряд (карбоксильная, фосфатная группа)
Молекула белка может обладать ОЧЕНЬ сложными хим свойствами и может выполнять ОЧЕНЬ сложные функции.
Благодаря особенностям своего хим строения, белки чрезвычайно разнообразны по своим хим свойствам и выполняемым в организме функциям
Функции:
выполняющиеся только белками:
1. каталитическая (ферментативная);
2. рецепторная;
3. транспортная:
1. пассивный транспорт (по градиенту) — канал;
2. активный транспорт — мембранный насос;
4. двигательная (актин, миозин);
очень важные:
5. регуляторная;
6. сигнальная;
7. защитная;
8. строительная (кератин);
вспомогательные:
9. запасная;
10.энергетическая.
Уровни организации
1) первичная структура – последовательность аминокислот;
2) вторичная структура: - α-спирали;
- β-листы. (многочисленные слабые водорондные связи, за счет которых происходит скручивание во вторичные структуры)
3) третичная структура – трёхмерные молекулы, образующиеся за счёт неиспользованных собственных зарядов. Гидрофобные связи – слабые, но стабильные за счёт количества. S-S связь – прочная, способная связывать молекулы и образовывать третичную структуру;
4) четвертичная структура (молекулярные комплексы). Классический пример - Гемоглобин.(состоит из 2 молекул α-глобина, 2 молекул β -глобина, гемма и иона железа.)
Со вторичной структуры начинается конформация молекул под температурой. Фактором, на неё влияющим, является концентрация различных ионов. Изменив свою конформацию, белок может остаться в стабильном состоянии. Изменение конформации влияет на химические свойства молекулы – способности выполнять необходимую функцию.
В отличие от жиров и углеводов белки обладают огромным структурным разнообразием => биологические функции белков тоже поразительно разнообразны.
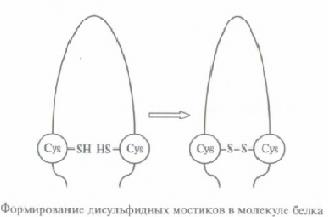
Одним из 20 вариантов аминокислот, используемых в составе белков, является цистин (Cys). В его радикале содержится функциональная группа SH. Если 2 остатка цистина в третичной структуре оказываются поблизости друг от друга, между ними, под действием особого фермента, может возникнуть дисульфидный мостик S-S.Такие мостики играют роль стяжек, стабилизирующих третичную структуру молекулы белка.
Функции конкретной белковой молекулы зависят не только от ее аминокислотной последовательности, но и от ее конформации в данный момент. (например, изменение конформации молекул белка посредством высокой температуры ведет к необратимой инактивации белка (сырое-вареное яйцо)).
Изменяя в своих клетках концентрацию некоторых ионов, организм способен тонко регулировать биологическую активность собственных белков. (кристаллы соли на яичном белке – мутные разводы – временная инактивация белков).
НУКЛЕИНОВЫЕ КИСЛОТЫ.
Сложные биополимеры, осуществляющие хранение и передачу генетической информации во всех живых организмах, а также участвующие в биосинтезе белков. Мономер нуклеиновой кислоты – нуклеотид. Главный смысловой компонент — азотистое основание — маленькая циклическая плоская
молекула жесткой формы. 
Как правило, в состав одной и той же молекулы кислоты входят нуклеотиды, содержащие либо только рибозу(ОН) либо только дизоксирибозу(Н), в соответствии с этим различают два типа нуклеиновых кислот:
1 – рибонуклеиновые кислоты
2 - дезоксирибонуклеиновые кислоты
2 – остаток фосфорной кислоты
3 – остаток азотистого основания Главным смысловым компонентом каждого нуклеотида является азотистое основание
Свойства азотистого основания: маленькая плоская молекула с жестко фиксированной формой. На этой молекуле имеются малые электростатические заряды
Благодаря строгому расположению мало-отрицательных и положительных зарядов, некоторые азотистые основания могут притягиваться друг к другу, образуя комплементарные пары (взаимно дополняющие)
У всех живых существ для образования молекул ДНК используется один и тот же универсальный набор из 4 типов нуклеотидов. Они отличаются друг от друга только азотистыми основаниями:
аденин (а)++++++ тимин (т)
гуанин (г) ++++++ цитозин (ц)
эти водородные связи слабые, но когда их много, они могут полотно удерживать молекулы.
Как правило, молекулы ДНК имеют двуцепочечное строение, причем, обе цепочки полностью комплементраны друг другу.
 ДНК: А-Г-А-Т-А-Ц-А-Ц-А
ДНК: А-Г-А-Т-А-Ц-А-Ц-А
А-Г-А-Т-А-Ц-А-Ц-А Т-Ц-Т-А-Т-Г-Т-Г-Т
 .........
.........
 Т-Ц-Т-А-Т-Г-Т-Г-Т
Т-Ц-Т-А-Т-Г-Т-Г-Т
Т-Ц-Т-А-Т-Г-Т-Г-Т
А-Г-А-Т-А-Ц-А-Ц-А
Благодаря особенностям своего химического строения, молекулы нуклеиновых кислот способны к точному воспроизведению (копированию). Этот процесс лежит в основе любого размножения. Организм сначала копирует свою генетическую информацию, а потом передает ее своим потомкам.
Определенные азотистые основания могут образовывать друг с другом комплементарные
пары. В составе одной и той же нуклеиновой кислоты обычно присутствуют нуклеотиды, в которых остатки моносахаридов представлены либо только рибозой, либо дезоксирибозой. Соответственно существует рибонуклеиновая кислота (РНК) и дезоксирибонуклеиновая (ДНК).
У всех живых существ в образовании молекул ДНК принимает участие стандартный набор азотистых оснований:
Аденин — Тимин
Гуанин — Цитозин
Молекула ДНК — две полностью комплементарные цепочки. Способность нуклеиновых
кислот к репликации обеспечивает наследственность.
Процедура репликации ДНК — очень сложный процесс, который не может идти
самопроизвольно. Он обеспечивается ферментом — ДНК-полимеразой.
Процесс реализации наследственной информации
