Действие галогенов
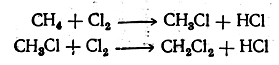

При этих реакциях хлор действует энергичнее других галоидов. Труднее всего реагирует иод, и притом реакция не идет до конца, так как, например, при взаимодействии метана с йодом образуется йодистый водород, реагирующий с йодистым метилом с образованием метана и иода (обратимая реакция):

Чтобы реакция дошла до конца, необходимо образующийся йодистый водород все время удалять из сферы реакции (па-пример, добавлением окиси ртути или йодноватой кислоты).
Действие азотной кислоты
Азотная кислота при обыкновенной температуре почти не действует на парафиновые углеводороды; при нагревании же действует главным образом как окислитель. Однако, как нашел М. И. Коновалов (1889), при нагревании азотная кислота действует отчасти и «нитрующим» образом; особенно хорошо идет реакция нитрования со слабой азотной кислотой при нагревании и повышенном давлении. Реакция нитрования выражается уравнением

т. е. один из атомов водорода заменяется на остаток NO2 (ни-трогруппа) и выделяется вода.
Особенности строения изомеров сильно отражаются на течении этой реакции, так как легче всего она ведет к замещению на нитрогруппу атома водорода в остатке СН (имеющемся лишь в некоторых изомерах), менее легко замещается водород в группе СН2 и еще труднее — в остатке СН3.Парафины довольно легко нитруются в газовой фазе при 150—475° С двуокисью азота или парами азотной кислоты; при этом происходит частично и. окисление. Нитрованием метана получается почти исключительно нитрометан:
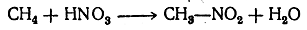
Последующие гомологи дают смесь различных нитропарафинов вследствие попутно идущего расщепления. При нитровании этана получаются нитроэтан СН3—СН2—NO2 и нитрометан СН3—NO2. Из пропана образуется смесьнитропарафинов:

Из нормального бутана:

Действие серной кислоты
Серная кислота при обыкновенной температуре не действует на парафины; при высокой температуре действует как окислитель. При слабом нагревании дымящая серная кислота может действовать на парафиновые углеводороды (особенно на углеводороды изострое-ния, содержащие группу СН), образуя сульфокислоту и воду (реакциясульфирования):
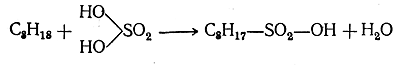
Одновременное действие сернистого ангидрида и кислорода
При совместном действии сернистого ангидрида и кислорода воздуха под влиянием ультрафиолетовых лучей или добавок перекисей парафиновые углеводороды, даже нормального строения, реагируют с образованием суль-фокислот (реакция сульфоокисления):

Одновременное действие сернистого ангидрида и хлора
При совместном действии сернистого ангидрида и хлора при освещении ультрафиолетовым излучением или под влиянием некоторых катализаторов происходит замещение атома водорода с образованием так называемых сульфохлоридов (реакция сульфохлорирования): Вместо смеси SO2 и Cl2 можно пользоваться хлористым сульфурилом.

Действие кислорода и окислителей
Кислород и окислители, даже такие сильные, как хромовая кислота и перманганат, при обыкновенной температуре почти не действуют на парафиновые углеводороды. При повышенной температуре сильные окислители медленно действуют на предельные углеводороды таким образом, что в каком-нибудь месте молекулы разрывается связь между атомами углерода и молекула распадается на отдельные осколки, окисляющиеся при этом в органические кислоты. Эти кислоты всегда содержат в молекуле меньшее число атомов углерода, чем исходный углеводород, т. е. реакции окисления являются всегда реакциями распада (расщепления) молекулы углеводорода.
Газообразный кислород при обыкновенной температуре воз-се или почти не действует на парафины. При высокой температуре углеводороды воспламеняются и горят, причем происходит полное разрушение органической молекулы, ведущее к образованию углекислого газа и воды. Лишь сравнительно недавно было исследовано действие кислорода и воздуха на алканы (преимущественно твердые) при средних температурах, когда окисление протекает довольно энергично, но не приводит к воспламенению. Оказалось, что и в этом случае происходит частичное расщепление молекул углеводородов с образованием кислородсодержащих веществ, главным образом органических кислот. В настоящее время окисление смеси высших твердых предельных углеводородов — окисление парафина - проводится в крупных промышленных масштабах для получения жирных кислот. В последнее время промышленное значение получает так называемое регулируемое (проводимое при сравнительно низких температурах) окисление кислородом или воздухом также и низших предельных углеводородов: метана, этана, пропана и бутана. При этом получаются смеси спиртов, альдегидов, кетонов и кислот, причем промежуточно образуются, очевидно, простейшие перекисные соединения. При окислении пропана, например, могут получаться следующие вещества:
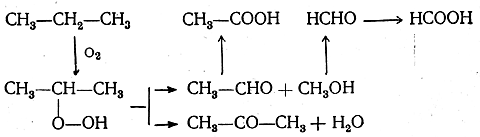
Обычно окисление пропана в промышленных условиях проводят таким образом, чтобы получить возможно больше ацетальдегида.
7. Действие высоких температур При высоких температурах все парафиновые углеводороды подвергаются более или менее глубокому распаду с разрывом связей С—С или С—Н. При этом образуются продукты, состав которых зависит от условий термического воздействия (температура, давление, продолжительность нагревания) и от природы углеводорода. Метан лучше всех других углеводородов выдерживает нагревание: он начинает заметно разлагаться лишь около 800° С. Важнейшим продуктом превращения метана является ацетилен, Одновременно получаются этилен к водород. Прпонижении температуры содержание ацетилена в продуктах распада понижается, а этилена — увеличивается; понижение давления способствует увеличению выхода обоих углеводородов. Выше 1600° С, а также при длительном нагревании до 800—1600° С метан распадается главным образом на углерод и водород.

Химические свойства непредельных углеводородов
| Алкены | Алкины | Алкадиены | |||
| 1. Основные реакции – реакции присоединения по месту разрыва кратной связи | |||||
| 1.1 Реакции гидрирования (гидрогенизации) – присоединение водорода | |||||
| СН2= СН – СН3+ Н2®СН3– СН2– СН3 пропен пропан | СН ºС – СН3+ Н2®СН2= СН – СН3 пропин пропен СН2= СН – СН3+ Н2®СН3– СН2– СН3 пропен пропан | Присоединение -1,4 (катализатор Ni) СН2= СН – СН = СН2+ Н2® бутадиен-1,3 ®СН3– СН = СН – СН3 бутен-2 | |||
| 1.2. Реакции галогенирования – присоединение галогенов. Качественная реакция на непредельные углеводороды – обесцвечивание бромной воды. | |||||
| СН2= СН – СН3+Br2®СН2Br– СНBr– СН3 пропен 1,2-дибромпропан | СН ºС – СН3+Cl2®СНCl = СCl– СН3 пропин 1,2-дихлорпропен СНCl= СCl– СН3+Cl2®СНCl– СCl– СН3 1,1,2,2-тетрахлорпропан | СН2= СН – СН = СН2+ Сl2® бутадиен-1,3 ®СН2Cl– СН = СН – СН2Cl 1,4-дихлорбутен-2 СН2– СН = СН – СН2+Cl2® ® СН2– СН – СН – СН2 1,2,3,4 - тетрахлорбутан ½ ½ ½ ½ Cl Cl Cl Cl | |||
| 1.3. Реакции гидрогалогенирования – присоединение галогеноводородов.. Правилу В.В. Марковникова: водород присоединяется к наиболее гидрогенизированному атому углерода (т.е. связанному с большим числом атомов водорода). | |||||
| Алкены | Алкины | Алкадиены | |||
| СН2= СН – СН3+ НBr®СН2– СНBr – СН3 пропен 2-бромпропан | СН ºС – СН3+HCl®СН2 = С Сl – СН3 пропин 2-хлорпропен СН2 Сl = С Сl – СН3+HCl®CH3–CCl2–CH3 ½ 2,2-дихлорпропан | СН2= СН – СН = СН2+ НСl® ® СН3– СН = СН – СН2Сl 1-хлорпропен-2 | |||
| 1.4. Реакции гидратации – присоединение воды. Катализатор – разбавленная Н2SO4. Для несимметричных непредельных соединений присоединение происходит по правилу Марковникова. | |||||
| СН2= СН – СН3+ НОН®СН2– СН – СН3 Пропен ½ ½ Н ОН пропанол-2 (спирт) | Эта реакция носит название "перегруппировка Кучерова". СН º С – СН3+HOH®[СН = С – СН3] ¾® CH3–C–CH3 пропанон (кетон) II пропин Hg2+НOH О | ||||
| 2. Термическое разложение. Реакция протекает при высокой температуре 600 – 10000С. | |||||
| С3Н6®3С + 3Н2 | С3Н4®3С + 2Н2 | С4Н8®4С + 4Н2 | |||
| 3. Реакции окисления | |||||
| 3.1.Полное окисление – горение С3Н6+ 4,5О2®3СО2+ 3Н2О 3.2. Частичное окисление (раствором перманганата калия КMnО4). СН2= СН–СН3+[O]+ НОН®СН2– СН – СН2 пропантриол-1,2,3, глицерин пропен ½ ½ ½ OН ОН ОН (трехатомный спирт) | Полное окисление – горение С3Н4+ 4О2®3СО2+ 2Н2О | Полное окисление – горение С4Н6+ 5,5О2®4СО2+ 3Н2О | |||
| Алкены | Алкины | Алкадиены | |||
| 4. Реакции полимеризации | |||||
| nСН2= СН – СН3®[– СН2– СН – ]n пропен ½ (пропилен) СН3 полипропилен | 4.1. Реакции тримеризации (образование аренов): 4000С, актив.уголь 3С2Н2 ¾¾¾®С6Н6 ацетилен бензол 3 СН ºС – СН3 ®С6Н3(СН3)3 пропин 1,3,5-триметилбензол | nСН2= СН – СН = СН2® бутадиен-1,3 ® [– СН2– СН = СН – СН2 –]n полибутадиен (бутадиеновый каучук) | |||
| |||||