Ферментативный гидролиз крахмала и гликогена осуществляется с помощью ферментов класса гидролаз, подкласса карбогидраз, называемых амилазами: a-амилазы, b-амилазы и глюкоамилазы. Различаются они по свойствам, распространению в природе и способу действия на крахмал. Наиболее активные амилазы содержатся в слюне и соке поджелудочной железы животных и человека, в плесневых грибах, проросшем зерне. Обычно препараты амилазы получают из высушенного проросшего зерна (солод).
Амилазы гидролизуют как неизмененные крахмальные зерна, так и крахмальный клейстер. Атакуемость крахмала амилазами увеличивается с уменьшением размеров крахмальных зерен, т.е. с увеличением их относительной поверхности. Она резко возрастает при механическом нарушении стуктуры крахмальных зерен. Действие амилаз усиливается на клейстеризованный крахмал. Поэтому в целом ряде отраслей пищевой промышленности, например, спиртовой, осахаривание крахмала солодом производится лишь после заваривания муки или измельченного картофеля.
a-амилаза – фермент, гидролизующий a-(1®4)-гликозидные связи внутри молекулы амилозы или амилопектина без определенного порядка. В результате образуются продукты неполного гидролиза крахмала – a-декстрины – полисахариды разной молекулярной массы.
В соотвествии со свойствами различают следующие виды декстринов:
1. амилодекстрины – окрашиваются раствором йода в фиолетово-синий цвет;
2. эритродекстрины, окрашиваются йодом в красно-бурый цвет;
3. ахродекстрины – окрашиваются йодом в слабо-желтый цвет;
4. мальтодекстрины – не дают окрашивания с йодом.
a-амилазу называют декстринирующим ферментом. Она не расщепляет a-(1®6) гликозидные связи.
При действием a-амилазы на амилозу можно получить при полном гидролизе около 85% мальтозы и 15% глюкозы, при действии на амилопектин – около 70% мальтозы, 10% изомальтозы (молекулы глюкозы связаны a-(1®6) гликозидной связью) и 20% глюкозы.
Схематически действие a-амилазы на крахмал можно представить:
а)амилоза:
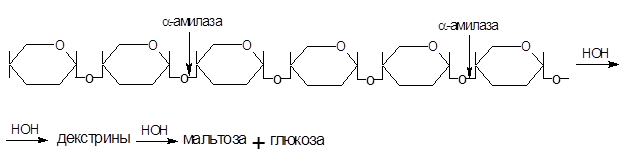
б) амилопектин
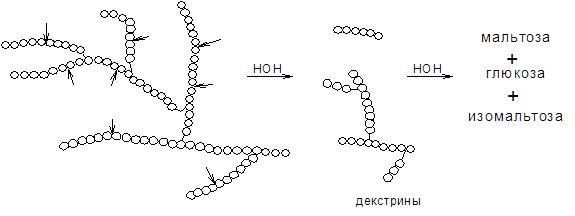
b-амилаза – фермент, который катализирует гидролиз крахмала и гликогена по a(1®4) гликозидной связи с нередуцирующих концов молекул. Она не расщепляет a(1®6) связи. В отличие от a-амилазы, b-амилаза действует упорядоченно и, начиная с нередуцирующего конца, отщепляет по молекуле мальтозы.
Амилозу b-амилаза расщепляет нацело, превращая ее на 100% в мальтозу. Если субстратом для действия b-амилазы служит амилопектин, то она расщепляет его на мальтозу и продукт неполного гидролиза, получивший название b-амилодекстрин, на оставшихся ответвлениях которого находятся a(1®6) гликозидные связи. Предельный декстрин гидролизуется b-амилазой только в том случае, если в реакционную смесь добавить a-амилазу. При совместном действии a- и b-амилаз на крахмал около 95% его превращается в мальтозу. Схема гидролиза крахмала под действием b-амилазы выглядит следующим образом:
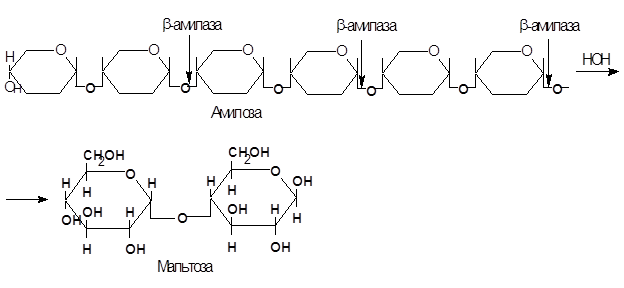
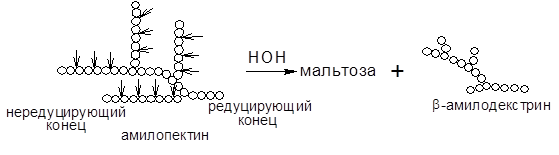
a- и b-амилазы различаются по своему отношению к реакции среды: a-амилаза гораздо более чувствительна к подкислению. Отличаются эти ферменты также по термостабильности и температурному оптимуму: a-амилаза более устойчива к действию повышенных температур, ее температурный оптимум (~70°С) лежит несколько выше, чем оптимум b-амилазы (50~60°С).
Амилазы имеют большое значение в хлебопекарной, пивоваренной, спиртовой промышленности. Брожение теста и накопление в нем СО2, разрыхляющего его и придающего хлебу равномерную пористость и хороший объем, зависят от присутствия в тесте сбраживаемых дрожжами сахаров. В свою очередь, содержание сахара в тесте зависит не только от количества сахара, находящегося в муке, но также от скорости накопления мальтозы при действии амилазы на крахмал. С другой стороны, слишком энергичное действие a-амилазы, имеющейся в большом количестве в муке из проросшего пшеничного или ржаного зерна, вызывает избыточное накопление в тесте декстринов, придающих мякишу хлеба плохую эластичность, заминаемость, недостаточную пористость и неприятный вкус.
Поскольку a-амилаза весьма чувствительна к повышению кислотности и резко понижает при этом свою активность, то тесто надо замешивать на так называемых жидких дрожжах или молочнокислых заквасках. Это обеспечивает накопление в тесте повышенного количества молочной кислоты, угнетающей a-амилазу и нежелательное образование декстринов.
Напротив, в пивоваренной промышленности конечные декстрины необходимы в сусле, поскольку в дальнейшем создают полноту вкуса пива, в определенной степени обусловливают его пеностойкость.
Глюкоамилаза – фермент, действующий с нередуцирующих концов амилозы и амилопектина, отщепляет молекулу глюкозы. Глюкоамилаза расщепляет не только a-1,4-, но и a-1,6-гликозидные связи. Амилоза и амилопектин полностью превращаются в глюкозу.
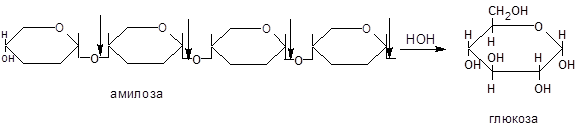
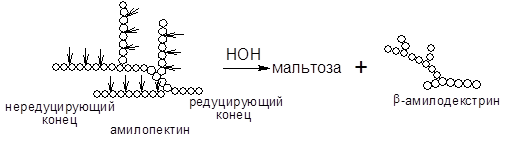
Глюкоамилаза встречается у микромицетов рода Aspergillus, Rhizopus, из которых производятся промышленные препараты глюкоамилазы. Применяется глюкоамилаза в крахмалопаточной промышленности для получения глюкозы и глюкозной патоки.
В молекуле амилопектина расщепление α(1→6)-связей катализирует амилопектин-1,6-глюкозидаза, которая действует на точки ветвления.
В результате совместного действия этих ферментов происходит полныйгидролиз крахмала до глюкозы.
Целлюлоза
Целлюлоза (клетчатка) – структурный полисахарид, является основным компонентом клеточных стенок растений.
Целлюлоза придает растительной ткани механическую прочность и эластичность, выполняя роль опорного материала растений. В природе целлюлоза не встречается в чистом виде. Волокна хлопка содержат 96-98% целлюлозы, в различных видах древесины содержание ее составляет 40-60%. Волокна льна и конопли состоят преимущественно из клетчатки. Важнейшими спутниками целлюлозы являются лигнин, гемицеллюлозы, пектиновые вещества, смолы и жиры.
Структурной единицей целлюлозы является b-D-глюкопираноза, звенья которой связаны b-(1→4)-гликозидными связями. Это подтверждается тем, что при частичном гидролизе клетчатки образуется дисахарид целлобиоза, имеющий тоже b-(1→4)-гликозидную связь. Строение клетчатки можно выразить следующей формулой:
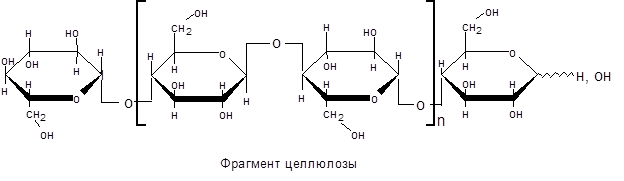 b-Д-глюкопираноза в составе клетчатки находится в креслообразной конформации. Это исключает возможность спирализации полиглюкозидной цепи, поэтому молекула целлюлозы сохраняет строго линейное строение.
b-Д-глюкопираноза в составе клетчатки находится в креслообразной конформации. Это исключает возможность спирализации полиглюкозидной цепи, поэтому молекула целлюлозы сохраняет строго линейное строение.
В растительных клеточных стенках молекулы целлюлозы связаны друг с другом бок о бок, образуя структурные единицы, получившие названия микрофибрилл.
Каждая микрофибрилла состоит из пучка молекул целлюлозы, расположенных по ее длине параллельно друг другу.Рентгеноструктурные исследования показали, что в полимерной цепи остатки молекул глюкозы повернуты относительно друг друга на 180°С, что делает возможным образование водородных связей между ОН-группой при атоме С-3 одного глюкозного остатка и кислородом пиранозного кольца следующего остатка глюкозы. Это препятствует вращению расположенных рядом остатков глюкозы вокруг соединяющей их гликозидной связи. В результате образуется жесткая линейная и пространственная структуры.
Целлюлоза не растворяется в воде, но в ней набухает. Она не усваивается организмом человека, т.к. в организме не вырабатывается фермент, способный расщеплять b-гликозидную связь. Однако она является необходимым для нормального питания балластным веществом, выполняющим энтеросорбентную функцию. Целлюлоза усваивается травоядными животными, в желудочно-кишечном тракте которых находится специфическая микрофлора, вырабатывающая фермент целлюлазу.
Схему гидролиза целлюлозы можно представить:
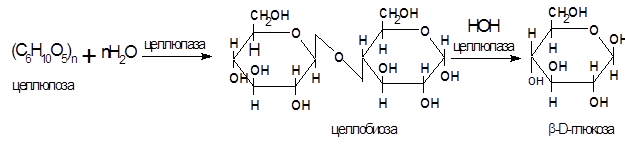 Кислотный гидролиз целлюлозы при температуре 170°С приводит к образованию глюкозы, которая используется для получения кормовых дрожжей, этилового спирта. В промышленности из целлюлозы получают хлопчатобумажные ткани, бумагу и целый ряд химических продуктов: вискозу, целлоффан, кинопленку, ацетатный шелк и др.
Кислотный гидролиз целлюлозы при температуре 170°С приводит к образованию глюкозы, которая используется для получения кормовых дрожжей, этилового спирта. В промышленности из целлюлозы получают хлопчатобумажные ткани, бумагу и целый ряд химических продуктов: вискозу, целлоффан, кинопленку, ацетатный шелк и др.
Гемицеллюлозы
Гемицеллюлозы – это сложная смесь полисахаридов, не растворяющихся в воде, но растворимых в щелочных растворах. Гемицеллюлозы всегда сопутствуют целлюлозе, в больших количествах содержатся в соломе, семенах, отрубях, кукурузных початках, древесине. В комплексе с целлюлозой выполняют структурную функцию.Гемицеллюлозы могут быть подразделены на гексозаны (маннаны, галактаны) и пентозаны (арабаны, ксиланы). Продуктами гидролиза у различных гемицеллюлоз являются манноза, галактоза, арабиноза, ксилоза.Гемицеллюлозы пшеничных отрубей – это высокоразвитые ксиланы, состоящие в основном из Д-ксилозы, L-арабинозы и глюкуроновой кислоты.
Из гемицеллюлоз промышленное применение нашли галактоманнаны, построенные из маннозы, образующей главную цепь, и галактозы, образующей короткие боковые цепи. Галактоманнаны обладают большой способностью связывать воду, поэтому они улучшают качество замеса, участвуют в формировании структуры теста, в частности, в формировании клейковины, тормозят черствение хлеба. Растворы галактоманнанов даже при концентрации 1% обладают высокой вязкостью, что объясняется вытянутой формой макромолекул и их склонностью образовывать в растворах крупные ассоциаты. Это свойство позволяет использовать их в качестве загустителей, стабилизаторов дисперсных систем, гелеобразователей.Галактоманнаны получают из семян бобовых культур.
Их используют при производстве различных пищевых продуктов, супов, соусов, мороженого, кремов, желе, напитков. Камеди и слизи. К полисахаридам близки камеди и слизи. В их состав входят сахара – арабиноза, ксилоза, галактоза, рамноза, а также глюкуроновая и галактуроновая кислоты.
Камеди образуют при набухании в воде вязкие гели или клейкие растворы, слизи при контакте с водой образуют слизистые массы. Камеди образуются в ответ на повреждения тканей растения в виде плотных блестящих натеков (вишневый, сливовый клей). Слизи содержатся в покровных тканях семян льна и зерновки ржи. Кроме защитной функции камеди и слизи могут повышать засухоустойчивость растения, способствуя удержанию влаги.Слизи имеют большое значение при переработке зерна ржи. Они повышают вязкость ржи при размоле, поэтому оно вымалывается труднее, чем пшеница и энергозатраты на размол у него выше. Слизи влияют на структурно-механические свойства в тесте, а, следовательно, и на качество хлеба. Мукополисахариды. Мукополисахариды получили свое название потому, что ряд веществ этого класса имеют слизистую консистенцию (от лат. mucus – слизь). Для мукополисахаридов характерно наличие их в молекулах значительного количества остатков аминосахаров и уроновых кислот. Это полисахариды соединительной ткани. Мукополисахариды обычно связаны с белками. Важнейшими представителями этой группы полисахаридов являются гиалуроновая кислота, хондроитин-серные кислоты и гепарин.
Гиалуроновая кислота построена из дисахаридных остатков, соединенных b-1,4-гликозидными связями. Дисахаридный фрагмент состоит из остатков D-глюкуроновой кислоты и N-ацетил-D-глюкозамина, связанных b-1,3-гликозидной связью:
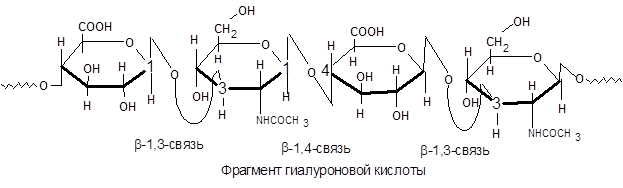 Гиалуроновая кислота имеет высокую молекулярную массу порядка 106, растворы ее обладают высокой вязкостью. Высокая вязкость гиалуроновой кислоты отчасти вызвана ее полианионным характером при физиологических значениях рН, которые способствуют гидратированию цепей и образованию между ними водородных связей. Вследствие высокой вязкости она понижает проницаемость тканевых оболочек и препятствует проникновению в ткани болезнетворных микроорганизмов. Особенно высоко ее содержание в коже, стекловидном теле глаза, сухожилиях. Гиалуроновой кислоте присущи не только структурные функции. Пронизывая ткани в качестве межклеточного вещества гиалуроновая кислота регулирует поступление в клетки тех соединений, которые или нужны для жизнедеятельности клетки или являются ее продуктом.
Гиалуроновая кислота имеет высокую молекулярную массу порядка 106, растворы ее обладают высокой вязкостью. Высокая вязкость гиалуроновой кислоты отчасти вызвана ее полианионным характером при физиологических значениях рН, которые способствуют гидратированию цепей и образованию между ними водородных связей. Вследствие высокой вязкости она понижает проницаемость тканевых оболочек и препятствует проникновению в ткани болезнетворных микроорганизмов. Особенно высоко ее содержание в коже, стекловидном теле глаза, сухожилиях. Гиалуроновой кислоте присущи не только структурные функции. Пронизывая ткани в качестве межклеточного вещества гиалуроновая кислота регулирует поступление в клетки тех соединений, которые или нужны для жизнедеятельности клетки или являются ее продуктом.
Хондроитинсульфат – непременная составляющая часть хряща, костной ткани, сухожилий, сердечных клапанов. Хондроитинсульфат прочно связан с белком коллагеном.
Хондроитинсульфаты состоят из дисахаридных остатков N-ацетилированного хондрозина, соединенных b-1,4-гликозидными связями. В состав хондрозина входят D-глюкуроновая кислота и D-галактозамин, связанные между собой b-1,3-гликозидной связью.

Как свидетельствует само название, эти полисахариды являются эфирами серной кислоты (сульфатами). Сульфатная группа образует эфирную связь с гидрокисльной группой N-ацетил-D-галактозамина, находящейся либо в 4-м, либо в 6-м положении. Соответственно различают хондроитин-4-сульфат и хондроитин-6-сульфат.
Наличие дополнительных SO3-группировок сообщает еще больший полианионный характер хондроитинам.
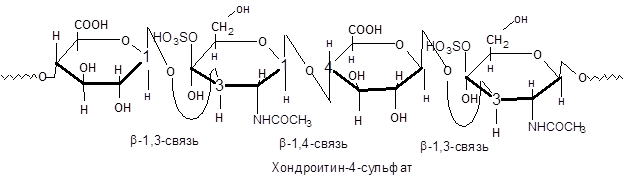
Гепарин – гетерополисахарид, широко распространенный в тканях животного организма и особенно в значительных количествах содержащийся в печени, сердце, мышцах и легких. Ничтожные количества гепарина задерживают свертывание крови, т.е. он является сильным природным антикоагулянтом. Благодаря этому гепарин получил практическое применение в медицине.Гепарин состоит из повторяющихся дисахаридных единиц, в состав которых входят остатки D-глюкозамина и двух уроновых кислот – D-глюкуроновой и L-идуроновой (преобладает). Внутри дисахаридного фрагмента осуществляется a-1,4-связь, если фрагмент оканчивается L-идуроновой кислотой, и b-1,4-связь, если D-глюкуроновой кислотой.Аминогруппа у большинства глюкозаминных остатков сульфатирована, а у некоторых из них – ацетилирована. 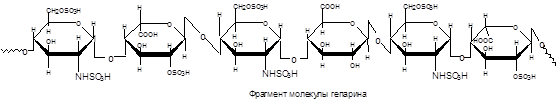
8. Пектиновые вещества – это соединения, состоящие главным образом, из метоксилированной полигалактуроновой кислоты. Остатки галактуроновой кислоты соединены a-1,4 гликозидной связью. Вместе с целлюлозой, гемицеллюлозой и лигнином пектиновые вещества образуют клеточные стенки растений, являясь цементирующим материалом этих стенок, объединяют клетки в единое целое в том или ином органе растений.
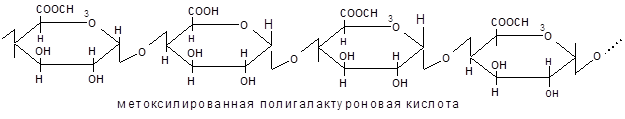 Различают три основные группы пектиновых веществ: протопектины, пектиновая кислота, пектаты, пектин.Для всех нерастворимых пектиновых веществ существует общее название – протопектин. Основным структурным компонентом протопектина служит галактуроновая кислота, из которой состоит главная цепь, в состав боковых цепей входят арабиноза, галактоза и рамноза. Часть кислотных групп галактуроновой кислоты этерифицирована метиловым спиртом.
Различают три основные группы пектиновых веществ: протопектины, пектиновая кислота, пектаты, пектин.Для всех нерастворимых пектиновых веществ существует общее название – протопектин. Основным структурным компонентом протопектина служит галактуроновая кислота, из которой состоит главная цепь, в состав боковых цепей входят арабиноза, галактоза и рамноза. Часть кислотных групп галактуроновой кислоты этерифицирована метиловым спиртом.
В общем виде структуру протопектина можно представить схематически:
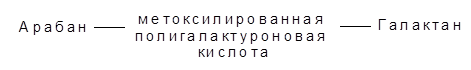
Протопектин легко расщепляется ферментом протопектиназой, переходя в растворимую форму – пектин. Пектином называют водорастворимое вещество, свободное от целлюлозы и гемицеллюлоз и состоящее из частично или полностью метоксилированных остатков полигалактуроновой кислоты (фрагмент структуры см. выше).Пектин содержит 100-200 остатков Д-галактуроновой кислоты. Определить степень метоксилирования затруднительно, так как эфирные связи при экстракции разрываются.При созревании и хранении плодов происходит переход нерастворимых форм пектина в растворимые. С этим явлением связано размягчение плодов. Пектиновая кислота – это цепь, состоящая из остатков Д-галактуроновой кислоты. Соли пектиновых кислот (чаще всего Са или Mg) называют пектатами. Большинство пектиновых кислот содержит от 5 до 100 этих остатков.
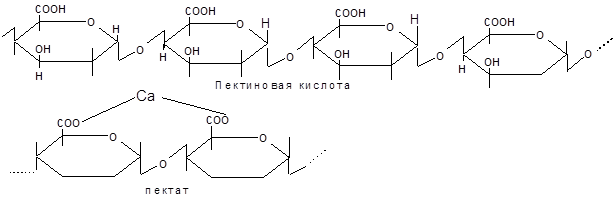 Пектиновые вещества содержатся в большом количестве в ягодах, плодах, клубнях. Важное свойство пектиновых веществ – способность их к желированию, т.е. свойство образовывать прочные студни в присутствии большого количества сахара (65-70%). Частичный гидролиз метиловых эфиров приводит к снижению желирующей способности. Пектиновая кислота не способна образовывать желе в присутствии сахара. Поэтому при промышленном получении пектиновых веществ процесс выделения пектина необходимо вести так, чтобы избежать гидролиза метоксильных групп, вызывающего снижение желирующей способности.На желирующей способности пектиновых веществ основано использование их в качестве студнеобразующего компонента в кондитерской промышленности для производства конфитюров, мармелада, пастилы, желе, джемов, а так же в консервной промышленности, хлебопечении.
Пектиновые вещества содержатся в большом количестве в ягодах, плодах, клубнях. Важное свойство пектиновых веществ – способность их к желированию, т.е. свойство образовывать прочные студни в присутствии большого количества сахара (65-70%). Частичный гидролиз метиловых эфиров приводит к снижению желирующей способности. Пектиновая кислота не способна образовывать желе в присутствии сахара. Поэтому при промышленном получении пектиновых веществ процесс выделения пектина необходимо вести так, чтобы избежать гидролиза метоксильных групп, вызывающего снижение желирующей способности.На желирующей способности пектиновых веществ основано использование их в качестве студнеобразующего компонента в кондитерской промышленности для производства конфитюров, мармелада, пастилы, желе, джемов, а так же в консервной промышленности, хлебопечении.
Пектиновые вещества играют в пищевой промышленности и отрицательную роль. В свеклосахарном производстве пектиновая кислота и пектин из свекловичной стружки переходят в диффузионный сок, в котором при его дальнейшей очистке с помощью известкового молока образуются пектаты кальция, в результате чего резко возрастает вязкость очищенного сока, что затрудняет его фильтрацию.Пектиновые вещества расщепляются под действием ряда ферментов: протопектиназы, пектинэстеразы, полигалактоуроназы.Схематически ферментативный гидролиз протопектина можно представить так:
