(общий алгоритм):
1. Понять и правильно записать условие
2. Для вещества, согласно условию задачи, подсчитать молярную массу
3. Определить количество этого вещества, используя соответствующую формулу (через весовые, объемные или структурные единицы).
4. Если в условии указано количество вещества, то ответ находим по производным формулам.
5. При этом необходимо помнить, что при решении должно соблюдаться соответствие между единицами измерения.
Нет необходимости заучивать формулы при решении задач, если вы понимаете, что означают и как связаны между собой данные в условии и искомые величины. Например, известен объем газа V. Количество газа можно найти, разделив объем газа на объем занимаемый одним молем:
n =  . Массу газа можно найти, умножив число молей газа на массу одного моля: m = n
. Массу газа можно найти, умножив число молей газа на массу одного моля: m = n 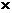 M =
M = 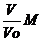 . Число молекул можно найти, умножив число молей на число молекул, содержащихся в 1 моле: N =
. Число молекул можно найти, умножив число молей на число молекул, содержащихся в 1 моле: N = 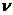
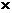 Na = Na
Na = Na 
Так можно вывести формулу для решения любой задачи
Связь между массой, количеством, числом молекул и объёмом газообразных веществ.
| Дано в условии | Требуется найти | Формула для расчета |
| Объём газа | Массу газа Число молей Число молекул | 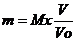 n =
n =  N=No
N=No 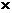 
|
Задачи с использованием количества вещества
Задача1. Какое количество, какую массу, и сколько молекул имеют 224 л азота?
Дано: Р е ш е н и е.
V(N2) =224 л 1. Объём газа связан с количеством вещества уравнением
Найти: n(N2)-? 
m(N2)-?
N(N2)-? n газ = 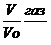 . Подставляя численные значения в уравнение
. Подставляя численные значения в уравнение
получаем:
М(N2) = 28 г/моль n(N2) = 224 / 22,4 =10 моль,
2. Масса вещества связана с количеством вещества и
объёмом:
m = n 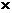
 M =
M = 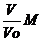 .
.
m = 10 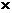
 28 = 280 г
28 = 280 г
3. Число молекул (структурных единиц) связано с
количеством вещества уравнением: N = Na 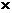 n = N a
n = N a  ,
,
подставляя значение в данное уравнение, находим
N (N2) = 6.02 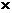 1023
1023 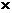
 10 = 60.2
10 = 60.2 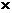
 1023 (молекул)
1023 (молекул)
Ответ: n(N2) = 10 моль; m = 280 г; N (N2) = 60.2 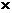
 1023 молекул
1023 молекул
Задача 2. Сколько молекул содержится в воде, количество
вещества которой равно 0,3 моль?
 |
Дано: Р е ш е н и е:
 n(Н2О) = 0,3 моль N(H2O) = n × NA - формула для расчета числа
n(Н2О) = 0,3 моль N(H2O) = n × NA - формула для расчета числа
N(структурных единиц)(Н2О) -? N(H2O) = 0,3 × 6,02×1023 = 1,8×1023 молекул
Ответ: N(H2O) = 1,8×1023 молекул
Задача 3. Вычислить массу и объем (н.у.) углекислого газа
количеством 5 моль.
Дано: Р е ш е н и е: 
 n(СО2) = 5 моль m(СО2) = n × M(СО2) = 5 × 44 = 220 г
n(СО2) = 5 моль m(СО2) = n × M(СО2) = 5 × 44 = 220 г
M(СО2) = 44 г/моль
 m(СО2) -? V(СО2) = n × VМ = 5 × 22,4 = 112 л
m(СО2) -? V(СО2) = n × VМ = 5 × 22,4 = 112 л
V(СО2) -?
Ответ: m(СО2) = 220 г, V(СО2) = 112 л.
Задача 4. Определить количество вещества атомного углерода,
содержащегося в карбиде кальция СаС2 массой 12,8 г
 |
 Дано: Р е ш е н и е:
Дано: Р е ш е н и е:
m(CaC2) = 12,8 г 1. Определяем количество вещества карбида

 кальция в данной массе:
кальция в данной массе:
n (C) -? n(CaC2) = m(CaC2) /М(СаС2) = 12,8/64 = 0,2 моль
М(СаС2)=64 г/моль 2. Находим соотношение между количеством
вещества углерода и количеством вещества
карбида кальция.
n (C) = 2n (CaC2) = 2∙0.2 = 0.4 моль
Ответ: 0,4 моль
Задача 5. Вычислить массовые доли элементов в нитрате натрия NaNO3
Р е ш е н и е:
 Дано: ω = Млемента n / Мвсей молекулы ∙100
Дано: ω = Млемента n / Мвсей молекулы ∙100
NaNO3
_________ М(NaNO3) = 85 г/моль
ω (Na)=? ω (Na)= М(Na) / М (NaNO3) ∙ 100
ω (N)=? ω (Na)= 23/85 ∙ 100 = 27,06 %
ω (O)=? ω (N)= М (N)/М(NaNO3)∙ 100
ω (N)= 14 / 85 100 = 16,47%
ω (O) = 3М(О)/М(NaNO3)∙ 100
ω (O) = 3∙ 16/ 85 ∙ 100 = 56,47 %
Ответ: ω (Na)=27,06%; ω (N)= 16,47 %; ω (O) = 56,47%
Алгоритм выполнения типовых заданий по теме «Эквивалент»