1.2.1. Вода как составная часть жидкостей организма
Основу жидкостей внутренней среды организма составляет вода. Общее содержание воды в организме взрослого человека составляет около 60— 65 % от массы его тела. При этом на долю внутриклеточной (интрацеллю- лярной) воды приходится 73, т. е. 40—45 % от массы тела, а остальное количество воды, составляющее 20—23 % от массы тела, распределено во внеклеточном пространстве. Из них около 16 % содержится в составе межклеточной жидкости (интерстициальная жидкость), 5 % — внутри сосудов, т. е. интравазально, в составе плазмы крови, 2 % — в лимфатических сосудах, в составе лимфы, 1—3 % воды от массы тела — в составе трансцеллю- лярных жидкостей.
Между всеми водными секторами организма осуществляется постоянный водный обмен (рис. 1.1)
Вода является растворителем всех органических и неорганических веществ, поступающих из внешней среды в организм и всасывающихся в желудочно-кишечном тракте. Вода, входящая в состав крови, интерстициальной жидкости и лимфы, переносит растворенные в ней питательные вещества к клеткам тканей и продукты обмена — к органам выделения. В воде, входящей в состав клеток организма, осуществляются все процессы обмена. Вода, благодаря высокой теплоемкости регуляции, обеспечивая выведение тепла из организма (теплоотдачу) с помощью потоотделения, испарения пота, тепловой одышки.
В крови, лимфе, трансцеллю- лярных жидкостях, пищеварительных соках вода находится в свободном, т. е. не связанном с органическими соединениями состоянии. В интерстициальном пространстве и клетках организма большая ее часть находится в связанном состоянии, т. е. связана с белками (например, с молекулами коллагена), другими органическими соединениями. Поэтому вода не вытекает при рассечении тканей органов.
Суточная потребность человека с массой тела 70 кг в воде составляет 2,5 л, из них 1,2 л поступает в организм человека в виде питьевой воды, 1 л с пищей, 0,3 л образуется при окислении жиров, белков и углеводов. Такое же количество воды (2,5 л) ежесуточно выводится из организма: с мочой до 1,5 л, с потом 0,5 л, с выдыхаемым воздухом 0,4 л, с калом 0,1 л. Вода в организме человека обновляется за 1 мес, а внеклеточная — за 1 нед. Недостаточное поступление воды в организм человека (например, если поступление воды в организм меньше ее объема, интенсивно выделяемого с потом на жаре) приводит к уменьшению воды в крови, интерстициальном пространстве. Это состояние называется дегидратацией. Дегидратация вызывает сгущение крови, повышение ее вязкости и, как следствие, нарушение кровообращения. Дегидратация, достигающая 20 % от массы тела, может привести к летальным последствиям.
1. 2.2. Гистогемати ческие барьеры
Между кровью и внеклеточным пространством находятся образования, получившие название гистогематических барьеров, отделяющие плазму крови от внеклеточной жидкости разных тканей организма. Последняя отделяется от внутриклеточной жидкости мембранами клеток. Гистогематиче- ские барьеры и мембраны клеток обладают избирательной проницаемостью для ионов и органических соединений. Поэтому электролитный и органический составы плазмы крови, внеклеточной и внутриклеточной жидкости различаются между собой.
По особенностям проницаемости для белков на уровне кровь — ткань все гистогематические барьеры делят на три группы: изолирующие, частично изолирующие и неизолирующие. К изолирующим барьерам относят гематоликворный (между ликвором и кровью), гематонейрональный, гема- тотестикулярный (между кровью и тестикулами), гематоэнцефалический (между кровью и мозговой тканью) и гематоофтальмический (между кровью и внутриглазной жидкостью), барьер хрусталика глаза. К частично изолирующим относятся барьеры на уровне желчных капилляров печени, коры надпочечников, пигментного эпителия глаза между сосудистой и сетчатой оболочками, щитовидной железы, концевых долек поджелудочной железы и гематоофтальмический барьер на уровне цилиарных отростков глаза. Неизолирующие барьеры хотя и позволяют белку проникать из крови в интерстициальную жидкость, однако ограничивают его транспорт в микроокружение и цитоплазму паренхиматозных клеток. Такие барьеры существуют в миокарде, скелетных мышцах, мозговом слое надпочечников, околощитовидных железах.
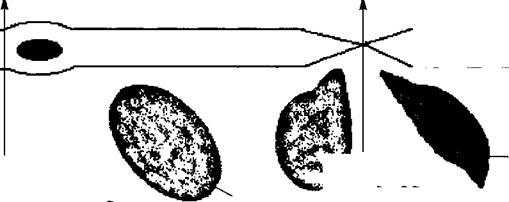
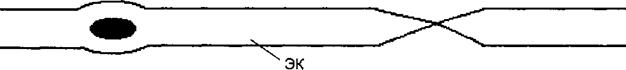
Структурным элементом гистогематических барьеров является стенка кровеносных капилляров. Морфологические и функциональные особенности клеток эндотелия капилляров — размер пор в их мембране, наличие фенестр, наличие межклеточного основного вещества, цементирующего щели между эндотелиоцитами капилляров и толщина базальной мембраны определяют проницаемость барьера для воды и растворенных в ней молекул веществ различных размеров и строения. Содержащиеся в крови вещества (вода, кислород, СО2, глюкоза, аминокислоты, мочевина и др.) могут проникать через барьер двумя путями (рис. 1.2): трансцеллюлярно (через клетки эндотелия) и парацеллюлярно (через межклеточное основное вещество).
Трансцеллюлярный транспорт веществ может быть пассивным (т. е. по концентрационному или электрохимическому градиенту без затрат энер-
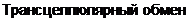

|
 |
|
|
|

 |
|
гии) и активным (против градиента с затратами энергии). Трансцеллюлярный перенос веществ осуществляется и с помощью пиноцитоза, т. е. процесса активного поглощения клетками пузырьков жидкости или коллоидных растворов. Парацеллюлярный транспорт, или перенос веществ через межклеточные щели, заполненные основным веществом, окутывающим волокнистые структуры фибриллярного белка, возможен для молекул разных размеров (от 2 до 30 нм), поскольку в капиллярах размеры межклеточных щелей неодинаковы. Базальная мембрана капилляров разных органов имеет неодинаковую толщину, а в некоторых тканях прерывиста. Эта структура барьера играет роль молекулярного фильтра, пропускающего молекулы определенного размера. В состав базальной мембраны входят гликозаминогликаны, способные уменьшать степень полимеризации и адсорбировать ферменты, повышающие проницаемость барьера. Снаружи в базальной мембране располагаются отростчатые клетки — перициты. Точных сведений о функции этих клеток нет, предполагается, что они выполняют опорную роль и продуцируют основное вещество базальной мембраны.
Основные функции гистогематических барьеров — защитная и регуляторная. Защитная функция заключается в задержке барьерами перехода вредных веществ эндогенной природы, а также чужеродных молекул из крови в интерстициальную среду и микроокружение клеток. При этом не только сама сосудистая стенка с ее избирательной проницаемостью, но и ячеисто-коллоидные структуры интерстиция, адсорбируя такие вещества, препятствуют их поступлению в микросреду клеток. Если же произошло проникновение крупномолекулярных чужеродных веществ в интерстициальное пространство и они не подверглись здесь адсорбции, фагоцитозу и распаду, то такие вещества поступают в лимфу, а не в клеточное микроокружение. Лимфа в этом плане представляет собой как бы «вторую линию обороны», поскольку содержащиеся в ней антитела, лимфоциты и моноциты обеспечивают обезвреживание чужеродных веществ.
Благодаря регуляторной функции гистогематические барьеры контролируют состав и концентрацию молекул различных соединений в интерстициальной жидкости, изменяя проницаемость барьеров для ионов, питательных веществ, медиаторов, цитокинов, гормонов, продуктов метаблиз- ма клеток. Таким образом гистогематические барьеры регулируют поступление различных веществ из крови в интерстициальную жидкость и своевременный отток продуктов клеточного обмена из межклеточного пространства в кровь.
Проницаемость гистогематических барьеров изменяется под влиянием вегетативной нервной системы (например, симпатические влияния уменьшают их проницаемость). Изменяют проницаемость гистогематических барьеров в сторону как увеличения, так и уменьшения циркулирующие в крови гормоны (например, кортикостероиды уменьшают проницаемость гематоэнцефалического барьера), тканевые биологически активные вещества (биогенные амины — серотонин, гистамин, гепарин и др.), ферменты (гиалуронидаза и др.), образуемые как самими эндотелиальными клетками, так и клеточными элементами интерстициального пространства. Например, гиалуронидаза — фермент, вызывающий деполимеризацию гиалуроновой кислоты основного вещества межклеточных пространств. Поэтому при его активации резко повышается проницаемость барьеров; серотонин — снижает их проницаемость, гистамин повышает ее; гепарин — ингибирует гиалуронидазу и в результате уменьшения ее активности снижает проницаемость барьеров; цитокиназы — активизируют плазминоген, и усиливая растворение фибриновых волокон, повышают проницаемость барьера. Повышают проницаемость барьеров метаболиты, вызывающие сдвиг pH в кислую сторону (например, молочная кислота).
Проницаемость гистогематических барьеров зависит и от химического строения молекул переносимых веществ, их физико-химических свойств. Так, для растворимых в липидах веществ гистогематические барьеры более проницаемы, поскольку такие молекулы легче проходят через липидные слои мембран клеток.
L2.3. Внутриклеточная жидкость
Во внутриклеточной жидкости преобладающими катионами являются калий (150 мэкв/л) и магний (40 мэкв/л), содержится большое количество ионов НРО7 (100 мэкв/л) и белков анионпротеинатов (т. е. молекул белка, имеющих отрицательный заряд) (55 мэкв/л). Столь высокие концентрации ионов калия во внутриклеточной жидкости связаны с их участием в биосинтезе белков и углеводов, магния — участием более чем в 300 энзимных внутриклеточных реакциях. Фосфатные ионы и анионпротеинаты входят в состав основных буферных систем, поддерживающих pH внутриклеточной жидкости. Осмотическое давление во внутриклеточной и внеклеточной жидкости примерно равно, что поддерживает постоянство объемов воды в этих секторах. Поэтому важнейшим следствием поддержания постоянства осмотического давления внеклеточной жидкости являетсй стабильность объема воды, содержащейся в клетках организма.
В отличие от внеклеточной жидкости, физико-химические показатели которой строго поддерживаются на постоянном уровне регуляторными механизмами, что и обеспечивает оптимальные условия для деятельности клеток организма, физико-химические показатели внутриклеточной жидкости характеризуются весьма широким диапазоном колебаний, которые обусловлены уровнем функциональной активности клеток. Так, при переходе клетки из ее нормального состояния в состояние возбуждения или торможения ее активности концентрация ионов — К, Mg, Са — в жидкой среде цитоплазмы резко изменяется. Например, концентрация ионов калия, являющаяся «жесткой» константой внеклеточной жидкости во внутриклеточной жидкости во время активации клеточной функции может изменяться от 115 до 150 мэкв/л. Концентрация ионов кальция в цитоплазме клетки, находящейся в состоянии физиологического покоя, составляет 10~7—10~8 моль/л, а при действии возбуждающего активность клетки сигнала (медиатора, гормона) концентрация Са++ в цитоплазме возрастает до 10~5—10~6 моль/л, т. е. в 20 раз. В то же время даже незначительное увеличение концентрации ионов Са во внеклеточной жидкости — с 1,2 до 1,4 ммоль/л, включает регуляторные механизмы, восстанавливающие нормальную концентрацию Са++ во внеклеточной жидкости.
1.2.4. Интерстициальная, или тканевая, жидкость
Около '/6 объема тела человека составляет пространство, расположенное между клетками организма, стенками кровеносных и лимфатических сосудов. Оно называется интерстициальным, или интерстициумом, а жидкость, заключенная в границах, образованных с одной стороны мембранами клеток, с другой — стенками кровеносных и лимфатических капилляров, называется интерстициальной, или тканевой, жидкостью. Как заметил К. Бернар, это «внутреннее море», в котором живут клетки.
Структура интерстиция представлена сетью коллагеновых и эластических волокон, филаментов протеогликанов. Коллагеновые волокна представляют собой белок, образуемый фиброцитами соединительной ткани. Масса коллагеновых волокон составляет 6 % массы тела, а общая поверхность этих волокон превышает 1 000 000 м2. Сеть этой своеобразной коллагеновой «губки» накапливает в интерстиции воду и электролиты, особенно натрий. Пучки волокон коллагена простираются вдоль всего интерстиция и обеспечивают механическую прочность (сопротивление) тканей. К плотным структурам интерстиция относятся также филаменты протеогликанов, очень тонкие и едва различимые в световом микроскопе. Их свернутые спиралью молекулы на 98 % состоят из гликозаминогликанов — гиалуроновой кислоты, хондроитинсульфатов А, В и С, а также белка. Молекулы протеогликанов и гликозаминогликанов имеют отрицательный заряд (анионы), благодаря чему поддерживается ионное равновесие с катионами интерстициальной жидкости.
Интерстициальная жидкость заключена в основном в мельчайших пространствах между филаментами протеогликанов и имеет характер геля. Поэтому ее еще называют тканевым гелем. Таким образом, филамент протеогликанов интерстиция формирует первую, коллоидную, или гелеподобную, фазу интерстиция, которая благодаря высокой гидрофильности связывает или освобождает воду под влиянием ферментов и биологически активных веществ (гиалуронидаза, гепарин, гистамин и др.). Быстрый транспорт молекул воды, О2, СО2, электролитов, питательных веществ, экскретов клеток между кровеносными капиллярами и клетками тканей обеспечивается простой диффузией через гель этих соединений. Скорость диффузии указанных веществ от стенок капилляров до клеток на расстоянии до 50 мкм осуществляется за несколько секунд. Вторая фаза интерстиция — водная, в виде свободной жидкости, «текущей» по тонким «каналам» вдоль коллагеновых волокон, составляет не более 1 % интерстициальной жидкости. При развитии отека (т. е. скопления воды и электролитов в межклеточном пространстве) содержание свободной жидкости в интерстициальном пространстве резко увеличивается, а «каналы» оказываются резко расширенными. В обеих фазах интерстициального пространства у взрослого человека содержится в среднем 11 — 12 л жидкости, т. е. около 16 % массы тела (см. рис. 1.1).
В ионном составе интерстициальной жидкости преобладают ионы натрия (142—144 мэкв/л) и ионы хлора (120 мэкв/л). Высокая суммарная концентрация данных ионов определяет величину осмотического давления интерстициальной жидкости. Поэтому при уменьшении концентрации Na в плазме крови и интерстициальной жидкости (например, при недостаточности коры надпочечников уменьшается секреция гормона альдостерона, усиливающего реабсорбцию Na+ в канальцах почек и Na+ в больших количествах с мочей выводится из организма) в интерстициальной жидкости появляется «осмотически свободная вода», которая выводится из организма через почки, а также по осмотическому градиенту диффундирует в клетки и вызывает их набухание. При увеличении же концентрации Na+ в интерстициальной жидкости (например, вследствие избыточного поступления NaCl в организм с соленой пищей) ее осмотическое давление повышается, вода задерживается в интерстициальном пространстве, что приводит к развитию отеков. Концентрация К+ в интерстиции (3,8—5 ммоль/л) в 30 раз меньше, чем во внутриклеточной жидкости. Это «жесткая» константа интерстициальной жидкости, и ее сдвиги вызывают нарушение функций клеток. Так, например, увеличение концентрации К+ в интерстициальной жидкости миокарда (следствие гиперкалиемии — увеличения концентрации К+ в плазме крови) уменьшает соотношение концентраций — К+ внутриклеточный / К внеклеточной жидкости, что приводит к деполяризации мембраны, нарушает восстановление мембранного потенциала клеток миокарда. В результате замедляется проведение возбуждения в сердечной мышце, что может вызвать остановку сердца. Жесткими константами являются и содержание Mg++ (0,75—1,2 ммоль/л) и Са++ (0,8—1,2 ммоль/л) во внеклеточной жидкости. Оба иона участвуют в поддержании нервно-мышечной возбудимости. Например, ионы Mg++ влияют на транспорт К+ через мембрану клетки и увеличение их концентрации во внеклеточной жидкости (следствие гипермагниемии) угнетает возбудимость нервной системы, скелетных мышц. Напротив, уменьшение концентрации Mg++ или Са++ в крови вызывает повышение нервно-мышечной возбудимости.
В интерстициальной жидкости содержится кислород, большое количество питательных веществ для клеток — глюкозы, аминокислот, жирных кислот, в ней содержится и СО2, поступающий из клеток и диффундирующий из интерстиция в кровь для удаления из организма, продукты белкового метаболизма клеток (мочевина, креатин, креатинин и др.). Из интерстициальной жидкости продукты обмена поступают в кровь и транспортируются ею к органам выделения — желудочно-кишечному тракту, почкам, которыми и выводятся из организма. Через поры капилляров соматического типа — их стенка представлена непрерывной базальной мембраной и эндотелиальным слоем, в которых имеются поры, шириной от 6 до 7 нм (в легких, коже) — в интерстиций способно выходить небольшое количество белков плазмы крови. Много большее количество их поступает в интерстициальное пространство через стенку капилляров синусоидного типа, представленных, например, в печени и имеющих эндотелиальный слой с фенестрами, базальную мембрану — с перерывами и в результате такой структурной организации — прерывистую стенку с большими просветами. Поэтому содержание белка неодинаково в интерстициальной жидкости разных тканей: оно низкое в подкожной ткани, в легких — 0,5—2 г/л. Однако в лимфе, оттекающей от интерстиция печени, в который из капилляров синусоидного типа поступает большое количество белка, содержание последнего достигает 55—60 г/л.
Общее количество белка во всем объеме интерстициальной жидкости организма (в 11—12 л) достигает 330—360 г. Отсюда, концентрация белка в 1 л интерстициальной жидкости составляет около 30 г/л и создает коллоидно-осмотическое (онкотическое) давление, равное 8 мм рт. ст., являющееся силой, удерживающей жидкость в интерстиции.
Все белки из интерстициальной жидкости возвращаются обратно в кровь только через лимфатическую систему. По пути кровь—лимфа—кровь за сутки рециркулирует от 50 до 100 % белка.
Давление интерстициальной жидкости оказывается на 3 мм рт. ст. меньше атмосферного. Причиной отрицательного давления интерстициальной жидкости по отношению к атмосферному давлению является постоянный отток жидкости из интерстиция по лимфатическим сосудам.
Интерстициальное пространство содержит клетки соединительной ткани — фибробласты и фиброциты, тучные клетки, макрофаги и лимфоциты, которые секретируют в микросреду клеток биологически активные соединения (ферменты, гепарин, биогенные амины, простагландины, лейкотриены, цитокины и др.), поддерживающие нормальное функциональное состояние интерстиция. Клетки интерстициального пространства осуществляют фагоцитоз, иммунную защиту интерстиция.
Микросреда клеток — это часть интерстициального пространства, непосредственно прилегающего к поверхности клеток, толщиной порядка 10— 20 нм, играет основную роль в обмене веществ через ее мембрану.
Микросреда клеток отличается от среды общего интерстициального пространства более высокой концентрацией поступающих из крови в интерстиций аминокислот и жирных кислот, используемых в пластических и энергетических процессах в клетке; медиаторов, гормонов и антигенов, регулирующих клеточные функции (пролиферацию, дифференциацию, метаболизм, синтез и секрецию антител и др.). Обмен воды и молекул между микросредой клеток и общим интерстициальным пространством происходит под влиянием градиентов сил гидростатического, онкотического и осмотического давления, электрокинетических и электростатических потенциалов. В создании последнего участвуют гликозаминогликаны, формирующие отрицательный заряд на поверхности мембран клеток.
Находящиеся в микросреде гуморальные факторы — нейромедиаторы, гормоны, метаболиты, цитокины, связываясь с их мембранными клеточными рецепторами, осуществляют физиологическую регуляцию различных функций клеток: процессов пролиферации и дифференцировки клеток, их метаболизма, например синтеза и продукции ими белков, гликопротеидов, липидов и других продуктов, что поддерживает постоянство структуры органов и тканей организма, обеспечивает приспособительную реакцию клеток к изменениям внешней среды.