| Фактор | Структура | Молекулярная масса полипептидов, кДа | Функция |
| P-TEFb | Гетеродимер | 124, 43 | Препятствует прекращению элонгации, ингибируется DRB |
| SII (TFIIS) | Мономер | Препятствует прекращению элонгации, стимулирует расщепление транскрипта | |
| TFIIF | Гетеродимер | 30, 70 | Устраняет задержку элонгации РНК |
| Элонгин (SIII) | Гетеротример, включающий элонгины A, B и С | Та же | |
| Элонгин А | Активная субъединица | ||
| Элонгин В | Регуляторная субъединица | ||
| Элонгин С | Та же | ||
| ELL | Устраняет задержку элонгации РНК | ||
| Примечание. DRB – 5,6-дихлоро-1-b- D -рибофуранозилбензимидазол |
выделенного в гомогенном состоянии из экстрактов Drosophila, подавляется нуклеотидным аналогом – DRB. Фенотипическим проявлением действия этого ингибитора является общее подавление синтеза гяРНК в ядрах вследствие резкого повышения частоты перехода элонгирующего комплекса в состояние полного прекращения транскрипции вблизи промоторов. DRB не подавляет элонгацию цепей РНК в бесклеточных системах транскрипции, реконструированных из высокоочищенных компонентов, что дало основание предполагать наличие дополнительных факторов, которые контролируют процесс перехода комплексов РНК-полимеразы II в фазу элонгации и чувствительны к действию этого ингибитора. Фактор P-TEFb оказался белком, обладающим именно такими свойствами. Механизм действия P-TEFb, благодаря которому этот фактор препятствует прекращению транскрипции РНК-полимеразой II, неизвестен. Предполагают, что он может быть связан с фосфорилированием РНК-полимеразы II или сопутствующих факторов транскрипции.
Небольшой белковый фактор SII, впервые выделенный из клеток асцитной опухоли Эрлиха, обеспечивает преодоление РНК-полимеразой II препятствий в виде нуклеопротеиновых комплексов или специфических последовательностей ДНК, вызывающих преждевременное прекращение транскрипции в кодирующих частях генов. Однако он не оказывает влияния на РНК-полимеразу, прекратившую элонгацию в DRB-чувствительной фазе. Фактор SII стимулирует эндонуклеазное отщепление 3’-концевой части транскрипта в комплексе, прекратившем элонгацию, что дает возможность РНК-полимеразе II продолжить элонгацию цепи РНК. Активный сайт РНК-полимеразы, обладающий такой эндонуклеазной активностью, ингибируется a-аманитином – специфическим ингибитором РНК-полимеразы II эукариот. Клетки дрожжей, у которых фактор SII инактивирован под действием мутаций, обладают повышенной чувствительностью к 6-азаурацилу и микофеноловой кислоте, которые, как известно, ингибируют биосинтез нуклеотидов, понижая внутриклеточное содержание GTP и UTP. Это, в свою очередь, оказывает сильное влияние на эффективность элонгации РНК РНК-полимеразой II в мутантных клетках.
Другая группа основных факторов элонгации супрессирует задержку элонгации цепей РНК, тем самым уменьшая вероятность перехода элонгирующих комплексов в состояние полного прекращения элонгации. Эту группу составляют три структурно неродственных белка: факторы TFIIF, элонгин (SIII) и ELL, которые, по-видимому, взаимодействуют непосредственно с компонентами тройного элонгирующего комплекса. Ни один из этих белков не способен реактивировать комплексы, полностью прекратившие транскрипцию, или стимулировать расщепление РНК в этих комплексах. Точный механизм супрессирующего действия данных факторов на задержку элонгации неизвестен. Недавно было установлено, что и элонгин, и фактор TFIIF резко повышают способность РНК-полимеразы II осуществлять зависимое от матрицы присоединение рибонуклеозидтрифосфатов к 3’-OH-концам фрагментов ДНК, которые в этом случае выполняют функцию праймеров. Предполагают, что роль элонгина и фактора TFIIF может заключаться в обеспечении правильного расположения в активном центре элонгирующего фермента 3’-OH-концов растущих транскриптов. Фактор TFIIF занимает особое место среди других основных факторов транскрипции, поскольку только он обладает способностью контролировать активность РНК-полимеразы II как на стадии инициации транскрипции, так и в фазе элонгации. При этом способность этого фактора оказывать действие на инициацию транскрипции или элонгацию контролируется разными доменами его полипептидных цепей.
Элонгин (SIII) впервые был выделен из ядер печени крыс в виде белкового комплекса, состоящего из трех субъединиц A, B и C с молекулярными массами ~150, 18 и 15 кДа соответственно. Транскрипционная активность элонгина (SIII) целиком ассоциирована с его A-субъединицей, а две другие служат регуляторными и после образования стабильного димера оказывают сильное стимулирующее действие на транскрипционную активность A-субъединицы. Собственно стимулятором активности элонгина А является элонгин C, тогда как элонгин B, гомологичный убиквитину, не взаимодействует стабильно с элонгином А в отсутствие элонгина С и выполняет шапероноподобную функцию при сборке всего комплекса элонгина (SIII). На особую роль элонгина (SIII) в регуляции экспрессии генов указывает тот факт, что у человека он известен как потенциальная мишень действия продукта антионкогена (гена-супрессора опухолей) von Hippel–Lindau (VHL), мутации в котором ассоциированы с возникновением многих видов рака у человека. Белок VHL специфически взаимодействует с комплексом элонгина BC, препятствуя его связыванию с элонгином А. При этом мутации в антионкогене, сопровождающие онкологические заболевания, уменьшают прочность взаимодействия мутантного белка с элонгином BC.
Ген фактора элонгации ELL (eleven–nineteen lysine-rich leukemia) человека, локализованный на хромосоме 19 (19p13.1), первоначально был обнаружен в связи с его частыми транслокациями в ген MLL (mixed lineage leukemia) на хромосому 11 (11q23) при острых миелоидных лейкозах. Предполагают, что продукт гена MLL участвует в регуляции транскрипции гомеозисных генов. В результате транслокации образуется "онкоген", кодирующий гибридный белок, который образован почти полным полипептидом ELL, объединенным с N-концевой частью белка MLL. Роль белка ELL в развитии лейкозов неясна, поскольку в настоящее время обнаружены шесть других генов, претерпевающих транслокацию в то же самое место на хромосоме 11, которые ассоциированы с лейкозами с различными клиническими проявлениями, характер которых зависит от природы транслоцируемого гена.
Терминация транскрипции. Прекращение синтеза РНК под действием РНК-полимеразы и освобождение РНК из транскрипционного комплекса происходят в конце транскрипционных единиц на особых участках ДНК - терминаторах транскрипции. Терминаторы транскрипции, функционирующие с разной эффективностью, могут находиться и внутри транскриптонов. Такие терминаторы являются мощными факторами, регулирующими уровень транскрипции (и других этапов экспрессии) соответствующих генов. Для осуществления терминации транскрипции на некоторых терминаторах РНК-полимеразам не требуется дополнительных белковых факторов, тогда как другие терминаторы в их отсутствие не функционируют.
Терминация транскрипции у бактерий. Типичные терминаторы, не требующие для своего распознавания РНК-полимеразой E. coli дополнительных белковых факторов, содержат GC-богатый участок, обладающий центральной симметрией, вслед за которым располагается последовательность нуклеотидов, состоящая из выстроенных подряд четырех–восьми остатков A, в матричной цепи ДНК. Транскрипция завершается на конце этой олиго(A)-последовательности или же на следующем за ней нуклеотиде. Предполагается, что после прохождения РНК-полимеразой GC-богатого участка ДНК с центральной симметрией в этом месте РНК образуется шпилька, что приводит к разрушению ДНК–РНК-гибрида в транскрибирующем комплексе.
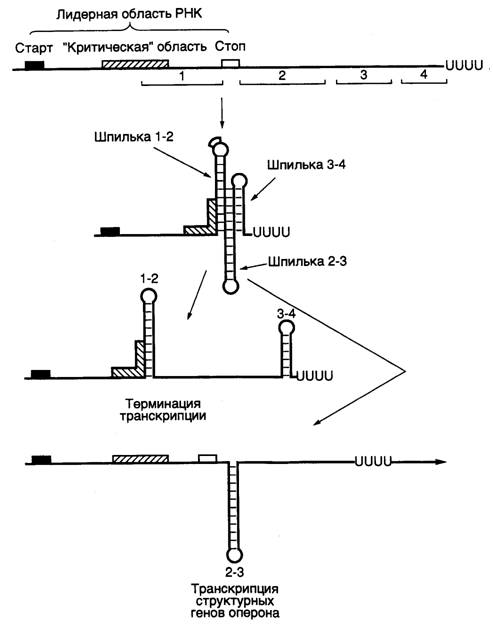
Рис. I.9. Аттенюатор триптофанового оперона E. coli и его функционирование
Изображены альтернативные вторичные структуры мРНК в районе аттенюатора, образование которых сопровождается прекращением транскрипции или распространением в область структурных генов оперона
Оставшаяся часть ДНК–РНК-гибрида нестабильна и легко плавится, поскольку образована 3’-концевой олиго(U)-последовательностью РНК и олиго(dA)-последовательностью терминатора. Первым из комплекса освобождается РНК-продукт, а затем минимальный фермент РНК-полимеразы. После объединения со свободным s-фактором образовавшийся холофермент РНК-полимеразы вступает в новый цикл транскрипции. Эффективность терминации транскрипции на таком терминаторе зависит от стабильности терминаторной шпильки РНК: мутации, нарушающие комплементарное спаривание оснований в шпильке, ослабляют терминацию, а мутации, восстанавливающие комплементарность, ее усиливают.
Кроме вышеописанного, у E. coli обнаружены терминаторы транскрипции, распознаваемые РНК-полимеразой только в присутствии белкового фактора терминации r, механизм действия которого хорошо изучен. Этот белок с молекулярной массой 46 кДа обладает РНК-зависимой нуклеозидтрифосфатазной активностью, которая необходима для его функционирования при терминации. Кроме того, для него характерна РНК:ДНК-хеликазная активность. Установлено, что фактор r связывается с растущей цепью РНК в особых неструктурированных участках, называемых рат-сайтами (rut sites, от англ. rut – колея, выбоина), до того, как РНК-полимераза достигает терминатора. В местах r-зависимой терминации транскрипции РНК-полимераза прекращает элонгацию. Считается, что роль r-фактора заключается в вытеснении РНК из транскрипционного комплекса во время таких пауз.
E. coliи другие бактерии имеют еще один тип регулируемых терминаторов транскрипции, называемых аттенюаторами. Впервые обнаружен и лучше других изучен аттенюатор триптофанового оперона, контролирующего биосинтез Trp в бактериальных клетках (см. рис. I.9). В условиях избытка внутриклеточного Trp девять из десяти молекул РНК-полимеразы, начавших транскрипцию триптофанового оперона, прекращают синтез РНК на аттенюаторе, расположенном на расстоянии в 180 п.о. от точки инициации транскрипции. В результате в основном происходит синтез коротких РНК той же длины, называемых лидерными. При уменьшении содержания Trp в клетках доля молекул РНК-полимеразы, преодолевающих аттенюатор, возрастает, что, в конечном счете, сопровождается увеличением внутриклеточного содержания ферментов биосинтеза Trp. Перед аттенюатором находятся несколько участков ДНК, последовательности которых обладают центральной симметрией. Это приводит к тому, что лидерная РНК, включающая в себя последовательности, комплементарные таким участкам, способна образовывать структуры типа шпилек в разных сочетаниях, которые исключают друг друга. Например, если получена шпилька 2/3, то шпильки 1/2 и 3/4 сформироваться уже не могут. К аналогичным результатам приводит и обратное развитие событий. Шпилька 3/4 является терминаторной, присутствующей в r-независимых терминаторах. За ней в лидерной РНК располагается последовательность олиго(U). Поэтому образование шпильки 3/4 сопровождается терминацией транскрипции на аттенюаторе и освобождением лидерной РНК из транскрипционного комплекса. Формирование альтернативных шпилек зависит от положения рибосом, транслирующих лидерную РНК с образованием лидерного пептида, в котором присутствуют два остатка Trp подряд. В условиях недостатка Trp рибосома в процессе синтеза лидерного пептида останавливается на соответствующих кодонах лидерной РНК, прикрывая собой последовательность 1, что препятствует формированию шпильки 1/2, так как образуется шпилька 2/3. В соответствии с этим терминаторная шпилька не может сформироваться, транскрипция не прерывается на аттенюаторе и РНК-полимераза переходит в область структурных генов оперона. Если недостаток триптофана не приводит к прекращению трансляции лидерной РНК, рибосома проходит критический участок лидерной РНК, препятствуя формированию шпильки 2/3, и образуется терминаторная шпилька 3/4, что сопровождается терминацией транскрипции на аттенюаторе.
Терминация транскрипции у эукариот. У эукариот обнаружены три фактора терминации транскрипции, необходимых для освобождения РНК-полимераз из транскрипционных комплексов на терминаторах – по одному для РНК-полимераз I, II и III. Белок N-TEF дрозофилы индуцирует освобождение транскриптов, синтезированных РНК-полимеразой II, и при его функционировании происходит расщепление ATP. У дрожжей белковый фактор Reb-1 связывается с природными терминаторами транскрипции на ДНК, обеспечивая как остановку элонгирующей РНК-полимеразы I на этих терминаторах, так и последующее освобождение РНК из транскрипционных комплексов. Удаление в результате делеции из рибосомной транскрипционной единицы Reb-1-связывающего сайта нарушает правильное образование 3’-концов рРНК in vivo. Мышиный фактор TTF-1, который также является ДНК-связывающим белком, необходим для правильной терминации транскрипции РНК-полимеразой I в клетках этих животных. У них же обнаружен LА-белок, специфически взаимодействующий с РНК, функционирование которого требуется для образования транскриптов полной длины под действием РНК-полимеразы III, что происходит в результате освобождения РНК из транскрипционных комплексов и реинициации транскрипции.
Рассмотрим подробнее механизм терминации транскрипции Pol I. У мышей терминация транскрипции рДНК происходит на 565 п.о. ниже кодирующей части гена 28S РНК. 3'-Конец терминирующего транскрипта картирован за 21 п.о. перед 18-нуклеотидным повтором, названным Sal-боксом (AGGTCGACCAGA/TT/ANTCCG), который входит в состав терминатора транскрипции. Десять таких повторов, фланкированных протяженными кластерами пиримидиновых оснований, локализованы в нетранскрибируемых спейсерах рДНК. У человека длина повтора составляет 11 п.о. (GGGTCGACCAG), и его последовательность соответствует таковой 5'-концевой части мышиного повтора. Последовательности, фланкирующие повторы, оказывают влияние на точность и эффективность терминации транскрипции, а функционирование всего терминатора зависит от его ориентации на ДНК.
С помощью мутационного анализа и футпринтинга было установлено, что фактор терминации транскрипции TTF-I взаимодействует с Sal-боксом и останавливает элонгирующую Pol I. Хотя все факторы терминации транскрипции, обсуждавшиеся выше, распознают разные последовательности нуклеотидов, для них характерно наличие в C-концевых частях двух ДНК-связывающих доменов длиной в 80 аминокислот каждый, гомологичных ДНК-связывающей последовательности онкобелка c-Myb. Хотя более половины полипептидной цепи с N-конца TTF-I могут быть удалены без потери его функций, одних лишь ДНК-связывающих доменов недостаточно для обеспечения белком терминации транскрипции, и для этого требуются прилегающие последовательности аминокислот. Факторы терминации транскрипции TTF-I мышей и Rib-1 дрожжей могут прекращать элонгацию цепей РНК на любой из этих ДНК. Это указывает на высокую эволюционную консервативность механизма терминации транскрипции Pol I.
Связываясь с последовательностями терминаторов, TTF-I изгибает молекулу ДНК и вызывает задержку элонгирующего транскрипционного комплекса на терминаторе. Предполагается, что в этот момент происходит конформационное изменение молекулы Pol I, что ослабляет взаимодействие компонентов комплекса друг с другом (как это имеет место в случае РНК-полимеразы E. coli на ρ-независимых терминаторах транскрипции). Окончательный распад комплекса и освобождение Pol I, а также синтезированной молекулы РНК происходит лишь в присутствии дополнительного фактора PTRF (polymerase and transcript release factor), который контактирует как с Pol I, так и с TTF-I.
Функциональная роль фактора TTF-I не ограничивается лишь участием в терминации транскрипции. Один из терминаторов транскрипции рДНК, так называемый To, расположен за 170 п.о. перед точкой инициации транскрипции генов рРНК. Взаимодействующий с To фактор TTF-I сильно стимулирует транскрипцию генов рРНК, вызывая перестройку структуры хроматина в окрестностях соответствующего промотора. Об изменениях структуры хроматина во время транскрипции см. следующий раздел 2.1.4.
Хотя для каждой из форм РНК-полимераз обнаружен свой специфический белковый фактор, необходимый для правильного освобождения транскриптов из элонгирующих комплексов, этим не ограничиваются механизмы, обеспечивающие терминацию транскрипции у эукариот. Действительно, одним из основных факторов терминации транскрипции у этой группы организмов является сложный белковый комплекс, обеспечивающий процессинг 3’-концевых последовательностей у предшественников мРНК, синтезируемых РНК-полимеразой II (см. ниже). В этом случае терминация транскрипции тесно сопряжена с процессингом пре-мРНК пока неизвестным молекулярным механизмом.
Терминация транскрипции митохондриальных ДНК человека, так же как и терминация синтеза рРНК, требует участия специального белкового фактора. В этом случае фактор mtTERM может ускорять терминацию транскрипции in vivo митохондриальной РНК-полимеразой, а также ферментами бактериального и фагового происхождения. В отличие от терминаторов генов рРНК, митохондриальные сигналы терминации транскрипции в комплексе с фактором mtTERM распознаются молекулами РНК-полимераз в обеих ориентациях, что делает возможной терминацию транскрипции на H- и L-цепях мтДНК. Вследствие этого один общий терминатор может обеспечивать сбалансированное образование продуктов транскрипции с обоих противоположно направленных митохондриальных промоторов.