Среди криогенных систем значительное место занимают такие, в которых используются не циклы, а разомкнутые процессы.
Для всех таких процессов в литературе, как правило, применяется термин «цикл», хотя, строго говоря, это неверно, поскольку параметры рабочего тела в начальной и конечной точках процесса здесь не совпадают, что для цикла − кругового процесса, как известно, обязательно. При этом смазывается и принципиальное различие между замкнутыми и разомкнутыми процессами.
Чтобы все же подчеркнуть это различие, иногда пользуются терминами «замкнутый цикл» и «разомкнутый цикл» (иногда «открытый цикл» и даже «разрывный цикл»). Однако и такие названия неправомерны, так как настоящий термодинамический цикл всегда замкнут, а «разомкнутый» цикл перестает быть циклом. Нелогичность этих словосочетаний обычно игнорируется; только в [3] специально оговаривается условность терминов «замкнутый цикл» и «разомкнутый цикл». С терминологической точки зрения выход из положения может быть найден посредством использования приставки «квази» («как бы», «похожий»), уже давно применяемой в термодинамике (например, квазиравновесный, квазистатический). Действительно, термины «квазицикл», «квазициклический процесс» показывают, что соответствующий процесс близок к циклу («как бы» цикл), но вместе с тем не совпадает с мим полностью.

Рис. 3-13. Простые разомкнутые процессы (а, г), квазициклы − прямой (б), обратный (д) и циклы − прямой (в) и обратный (е) в T, s-координатах.
Разница между циклом и квазициклом определяется тем, что первый представляет собой круговой процесс и, следовательно, всегда замкнут (обмен массой через границы системы отсутствует), а второй − разомкнутый процесс с обменом массой через контрольную поверхность системы.
Вместе с тем квазицикл принципиально отличается от всех других разомкнутых термодинамических процессов важным свойством, которое объединяет его с циклом − обязательным обменом через границы системы тепловыми потоками разного знака (т.е. наличием и теплоприемника, и теплоотдатчика). Другими словами, квазицикл, так же как и цикл, осуществляет перенос тепла (точнее, энтропии) с одного температурного уровня на другой с затратой (или получением) соответствующей работы. В разомкнутых процессах, не относящихся к квазициклам, такое преобразование невозможно, поскольку в них существует внешний теплообмен только одного знака. Этот вид разомкнутых процессов, не связанных с переносом тепла, также целесообразно определить отдельным термином. Поскольку он пока отсутствует, в дальнейшем будем называть их просто «разомкнутыми процессами» в отличие от квазициклов.
Таким образом, все термодинамические процессы в зависимости от характера внешнего обмена энергией и массой могут быть разделены на три класса: разомкнутые процессы, квазициклы и циклы.
Рассмотрим некоторые особенности квазициклов, определяющие их отличия от процессов двух других классов. Для этого представим их в общем виде в Т, s-координатах (рис. 3-13).
Процессы на диаграммах рис. 3-13, а и г − простые разомкнутые процессы. Они могут протекать как с увеличением энтропии (s 2> s 1 подвод тепла q’), так и с ее уменьшением (s 2< s 1 отвод тепла q’’); однако направление изменения энтропии рабочего тела в каждом случае неизменно (либо увеличение, либо уменьшение). В этом смысле простые разомкнутые процессы характеризуются однонаправленностью изменения s.
Квазициклы, представленные па диаграммах рис. 3-13, б и д,характеризуются в одной части (1-а) возрастанием энтропии (s a> s 1, подвод тепла q’), а с другой − уменьшением (s 2 >sa,отвод тепла q’’), причем эти изменения энтропии в общем случае могут быть неравны 1. Если часть процесса с повышением энтропии проходит при более высоких температурах, чем часть, где энтропия понижается, то квазицикл будет прямым; если более высокая температура соответствует уменьшению энтропии, то квазицикл будет обратным.
1 В частном случае у квазициклов  может быть и равной
может быть и равной  (показано штрихом на диаграммах).
(показано штрихом на диаграммах).
Наконец, на диаграммах рис, 3-13, в и е показаны прямой (в) и обратный (е) циклы. Здесь точки 1 и 2 обязательно совпадают и  .
.
Таким образом, первое различие определяется особенностями изменения энтропии рабочего тела в процессах каждого из трех классов.
Второе различие процессоврассматриваемых трех классов определяется особенностями их материального, энергетического и эксергетического балансов *.
Материальный баланс в разомкнутых процессах − как простом (однонаправленном), так и в квазицикле − характеризуется равенством поступающих и выходящих потоков рабочего тела
 (3-47)
(3-47)
Для циклов 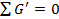 и
и  , поэтому вопрос о материальном балансе в этом классе систем отпадает.
, поэтому вопрос о материальном балансе в этом классе систем отпадает.
Энергетический баланс простого разомкнутого процесса имеет вид:
 (3-48)
(3-48)
 (3-48а)
(3-48а)
* Все балансы здесь и в дальнейшем относятся к стационарным (или квазистационарным) процессам; для нестационарных в принципе ничего не меняется, если учесть изменение массы и энергии системы.

Рис. 3-14. Обратный квазицикл с областью разрыва вблизи T o.с..
Параметры рабочего тела и точках 1 и 2 различны.
В процессах этого класса тепло может либо только подводиться, либо только отводиться: первому случаю соответствует уравнение (3-48), второму − (3-48а). Остальные величины, кроме членов, содержащих энтальпию, могут в зависимости от вида процесса быть как больше нуля, так и равными ему.
Энергетический баланс квазицикла имеет аналогичный вид, но в уравнение обязательно входят обе величины − подводимое тепло  и отводимое
и отводимое  :
:
 (3-49)
(3-49)
Энергетический баланс цикла отличается от уравнения (3-49) отсутствием  и
и  :
:
 . (3-50)
. (3-50)
Равенство (3-50) характеризует известное фундаментальное свойство цикла: суммы количеств работы и тепла на входе и выходе всегда равны. Для квазицикла, напротив, это равенство в общем случае не соблюдается:
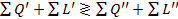 . (3-51)
. (3-51)
Только при  неравенство (3-51) сводится к неравенству (3-50).
неравенство (3-51) сводится к неравенству (3-50).
Эксергетические балансы процессов трех классов аналогичны уравнениям (3-49) − (3-51); разница состоит в том, что во всех случаях сумма отводимых потоков эксергии будет меньше, чем подводимых на величину  потерь от необратимости. Только в обратимых процессах
потерь от необратимости. Только в обратимых процессах 
Для простого (однонаправленного) разомкнутого процесса
 (3-52)
(3-52)
или
 (3-52а)
(3-52а)
где е − эксергия потока вещества;  –э ксергия теплового потока.
–э ксергия теплового потока.
Для квазицикла
 (3-53)
(3-53)
Для цикла
 (3-54)
(3-54)
Третье различие состоит в том, что влияние параметров окружающей среды в каждом случае принципиально различное. Для цикла важны только температуры внешних источников и приемников тепла; для квазициклов, напротив, важны как параметры теплоприемника и теплоотлатчика, таки давление р о.с.и температура Т о.с.среды (или других источников и приемников вещества, находящихся за пределами системы).
Квазициклы криогенных систем обычно имеют разрыв в области параметров р и Т, близких к р о.с.и Т о.с.. Схематично это показано нарис. 3-14 применительно к обратному квазициклу. Температура в точке 2 ниже, чем в точке 1 на величину D T н(D T недорекуперации).
Естественно, чем ближе точка 2 подойдет к точке 1 (т. е. чем больше квазицикл приблизится к циклу), тем меньше будет внешняя потеряот необратимости De, связанная с различием параметров выпускаемого потокаи окружающей среды. В общем случае это различие может существовать по трем параметрам − температуре, давленииi и составу.
Для анализа криогенных установок знание особенностей квазициклов имеет важное значение не только потому, что многие из них (D, L и некоторые R) представляют собой открытые системы. Низкотемпературные обратные циклы всегда частично расположены в области T > Т о.с. (только в этом случае возможен отвод тепла Q 0.c в окружающую среду). Поэтому при анализе оказывается удобным рассматривать низкотемпературную часть системы, работающую при T < Т о.с. (криоблок), отдельно от теплой части. В этом случае осуществляемые в ней процессы должны рассматриваться как квазицикл. Подробно этот вопрос рассмотрен в гл. 4.
Изложенные в этой главе разделы термодинамического анализа позволяют получить, зная необходимые термодинамические параметры рабочих тел, исходную термодинамическую информацию, необходимую при изучении существующих и разработке новых криогенных систем. Следует учитывать, что никакой, самый совершенный термодинамический аппарат в принципе не может точно показать, «что нужно делать» при создании новых систем и их элементов, когда нужны оригинальные, эвристические решения. Термодинамика, как и любая наука, может только показать «чего не нужно делать» и тем самым определить направление и существенно сузить область поиска. А это уже очень много!