Цель работы. Определение плотности энергии когезии (ПЭК) неполярного и полярного каучуков по данным набухания. Установление влияния степени полярности каучука на величину энергии когезии.
Краткая теория
Макромолекулы полимера представляют собой длинные цепочки из повторяющихся по химической природе звеньев. Звено макромолекулы содержит определенное число атомов разной химической природы, объединенные в некоторую химическую и пространственную структуру с помощью ковалентных (ионных, водородных) связей. Каждый атом звена имеет положительно заряженное ядро и отрицательно заряженную многоуровневую электронную оболочку. Движение электронов по орбиталям вокруг ядра приводит к возникновению диполей с очень коротким временем «жизни».
Взаимодействие этих диполей определяет появление так называемых дисперсионных связей внутри - и/или межмолекулярного характера. Каждый атом, входящий в состав звена макромолекулы имеет свою электронную плотность в соответствии со своей химической природой и природой звена в целом. По этой причине звено макромолекулы имеет постоянный электрический диполь, величина которого зависит от его химической природы и пространственного расположения атомов. Постоянные диполи «своих» и «чужих» звеньев макромолекул взаимодействуют между собой, образуя ориентационные связи.
Еще один тип физических ван-дер-ваальсовых связей возникает, когда «сильный» постоянный диполь одного звена макромолекулы наводит за счет поляризации диполь в другом звене.
Такой тип связи называется индукционным. Наиболее большой по энергии взаимодействия среди физических связей является водородная связь, которая образуется между сильно электроотрицательными атомами (F,O, N, S, Cl) и атомами водорода.
Для оценки величины суммарного межмолекулярного взаимодействия полимерных молекул пользуются величиной плотности энергии когезии. Применительно к низкомолекулярным жидкостям ПЭК определяется как молярная энергия испарения, деленная на молярный объем. Для каждой низкомолекулярной жидкости известен или может быть рассчитан параметр растворимости s, который равен квадратному корню из плотности энергии когезии:
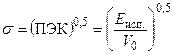 . (13)
. (13)
Для полимеров параметр растворимости определяют обычно из данных по равновесному набуханию. Параметры растворимости полимера и растворителя равны, если для данного растворителя наблюдается максимально возможная степень набухания полимера. Поэтому, определив степень набухания полимера в ряду растворителей с известными значениями s р , строят зависимость величины степени набухания полимера от параметра растворимости растворителя. При этом получают кривую, напоминающую по виду гауссову, центрированную относительно некоторого значения параметра растворимости s, при котором набухание максимально. Лучшим считается тот растворитель, в котором степень набухания максимальна при условии отсутствия теплового эффекта смешения или изменения объема системы. Суммарная энергия межмолекулярного взаимодействия складывается из энергий ориентационного, индукционного, дисперсионного и водородного взаимодействий. Вклад каждого вида взаимодействий может быть различным и зависит от природы полимера. В системе слабополярных макромолекул основными являются силы дисперсионного взаимодействия, но с увеличением полярности молекул все большее значение приобретают силы ориентационного взаимодействия.
Значение ПЭК зависит от химической структуры полимера. Полимеры, имеющие более сложную структуру звена, как правило, обладают большим значением ПЭК, и наоборот.
Интенсивность межмолекулярного взаимодействия является решающим фактором, лежащим в основе разделения полимеров на эластомеры, пластомеры и волокна. ВМС с наиболее интенсивными межмолекулярными взаимодействиями, склонные к образованию упорядоченных областей, являются типичными волокнообразующими материалами. Для них ПЭК может достигать весьма высоких значений. Влияние регулярности структуры и энтропийного фактора служит причиной возможного исключения из этих закономерностей.
Из значения плотности энергии когезии каучука можно найти параметр его растворимости σ к:
 . (14)
. (14)
Для определения численного значения ПЭК каучука по данным равновесного набухания строится графическая зависимость в координатах: степень набухания полимера Q р – параметр растворимости растворителя σ р.
Построенная кривая имеет максимум, соответствующий по оси абсцисс параметру растворимости полимера σ к:
|
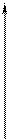

|

sк
Рис. 17. Типичный график зависимости количества поглощенного
растворителя от параметра растворимости растворителя
Методика эксперимента
Посуда, реквизиты и образцы: аналитичекие весы, бюксы, эфир, толуол, гептан, гексан, дихлорэтан, изопропиловый спирт, ацетон, тетрахлорметан, другие растворители, вулканизаты каучуков СКИ-3 и СКН-40, секундомер, пинцет, фильтровальная бумага.
В эксперименте используются слабо структурированные ненаполненные вулканизаты, которые способны хорошо набухать в ряде растворителей, но не растворяться в них из-за наличия поперечных связей. Для определения ПЭК берут вулканизаты двух каучуков и растворители согласно рекомендациям таблицы 4. Образцы вулканизатов каучуков вырезают в виде квадратиков размером 3´3 мм.
Для каждого изучаемого вулканизата вырезаются 5 одинаковых образцов. Каждый образец взвешивают на аналитических весах и помещают в бюкс, куда вносится по 8 мл одного из растворителей, рекомендованных в таблице. Каждый из бюксов номеруется. В рабочей тетради, согласно номеру бюкса, фиксируется тип полимера и растворителя, а так же вес исходного вулканизата – m 0.
Бюксы, с содержащимся в них полимером и растворителями, оставляют до следующего занятия, но не менее чем на две недели. Бюксы желательно убрать в шкаф, поставив их на бумагу с надписью, указывающей фамилии и № группы студентов, дату выполнения работы.
Через две недели каждый из образцов поочередно вынимают пинцетом из бюксов, обмакивают в эфир, промокают фильтровальной бумагой, замечают по секундомеру время, и по истечении 30 секунд образец взвешивают на весах, определяя массу набухшего образца m н.
Объемную степень набухания в условиях равновесия (Q p) рассчитывают по формуле:
 , (15)
, (15)
значения r к и r р находим из таблицы 5.
По результатам эксперимента заполняется таблица 3.
Таблица 3
Зависимость объемной степени набухания каучука от растворителя
| Растворитель | r р , г/см3 | s р, (МДж/м3)1/2 | m 0 , г | m н, г | Q р |
Для нахождения параметра растворимости полимера строят графическую зависимость (Q р; s р), и точка максимума на кривой соответствует параметру растворимости полимера s к, следовательно, согласно уравнению (14),
 .
.
Таблица 4
Рекомендуемые типы растворителей для определения плотности энергии когезии разных каучуков
| Каучук | Раствори- тели | s (МДж/м3) 0,5 | Каучук | Растворители | s (МДж/м3) 0,5 |
| Натуральный | Пентан | 14,19 | Бутадиен–нитрильный СКН–40 | Бензол | 18,86 |
| Октан | 15,546 | Хлорбензол | 19,43 | ||
| Циклогексан | 16,875 | Этилацетат | 18,61 | ||
| Толуол | 18,35 | Ацетон | 19,92 | ||
| Бензол | 18,86 | Этиловый спирт | 26,33 | ||
| C CL4 | 17,65 | 1,2–дихлорэтан | 20,37 | ||
| Бутилкаучук | Пентан | 14,2 | Полисульфидный | Толуол | 18,35 |
| Гептан | 15,3 | Бензол | 18,86 | ||
| Октан | 15,55 | Хлорбензол | 19,43 | ||
| Циклогексан | 16,88 | Бутиловый спирт | 22,03 | ||
| П. –ксилол | 18, 47 | ||||
| Хлоропреновый | Циклогексан | 16,875 | Силоксановый | Пентан | 14,2 |
| П. –ксилол | 18,47 | Гексан | 14,99 | ||
| О. –ксилол | 18,47 | Гептан | 15,3 | ||
| Бензол | 18,86 | Октан | 15,55 | ||
| 1,2–дихлорэтан | 20,37 |
Таблица 5 Плотности растворителей и каучуков
| Растворитель | r р , г/см3 | Растворитель | r р , г/см3 |
| Ацетон | 0,79 | Толуол | 0,88 |
| Бензол | 0,88 | Трихлорметан | 1,50 |
| Бутиловый спирт | 0,81 | Тетрахлорметан | 1,60 |
| Гексан | 0,66 | Эфир диэтиловый | 0,79 |
| Гептан | 0,68 | Этиловый спирт | 0,79 |
| Дихлорэтан | 1,25 | Этилацетат | 0,90 |
| Ксилол (о. -, п. -) | 0,88 | Циклогексан | 0,78 |
| Каучук | r к , г/см3 | Каучук | r к , г/см3 |
| СКИ-3 | 0,92 | СКН–40 | 0,97 |
Обсуждение полученных результатов
Вначале данного раздела студенту следует дать краткое определение понятию плотности энергии когезии. Затем, по построенному графику зависимости Qp = f(σ p) найти значение параметра растворимости каучуков σк, при котором объемная степень набухания максимальна. На занятии выдаются вулканизаты на основе малополярного каучука СКИ-3 и сильно полярного СКН-40.
Анализируя полученные данные, нужно сравнить значения ПЭК резин на основе каучуков СКИ-3 и СКН-40. Ключевым моментом данной работы является выведение качественной зависимости ПЭК от химической структуры полимера. Под химической структурой полимера подразумевается рассмотрение, главным образом, наличия в макромолекулах полярных атомов или групп, а также влияние степени разветвленности и длины макроцепи. На силу межмолекулярных взаимодействий также влияют типы связей, которые образует полимер с растворителем.
Поскольку энергия связи возрастает с повышением поляризуемости и дипольного момента, требуется привести значения показателей, характеризующих силу притяжения между группами в полимере. Одним из таких показателей является константа
притяжения G i. Существенное влияние на данный показатель оказывают наличие двойных связей и степень разветвленности макроцепи. Необходимо выявить зависимость между показателем G i и параметром растворимости полимера.
Пример. СКИ-3- каучук, дипольный момент которого близок к нулю. Объемная степень набухания Q p в полярном растворителе имеет практически минимальное значение.
Значение константы притяжения групп заместителей в полимере составляет G i = (-CН3 -) =438 (мк ∙ Дж ∙ м3)0,5, а G i = (-CN-) =838 (мк ∙ Дж ∙ м3)0,5, что обусловлено присутствием –СN- группы в бутадиен-нитрильном каучуке. Таким образом, для удаления взаимодействующих молекул на расстояние, при котором будет отсутствовать межмолекулярное взаимодействие необходимо меньшее количество работы в случае использования СКИ-3 по сравнению с СКН-40, соответственно значение ПЭК изопренового каучука будет меньшим.
Выводы
Кратко и лаконично перечисляются основные итоги раздела «Обсуждение результатов». По экспериментальным данным определяется значения ПЭК для каучуков СКИ-3 и СКН-40. Вывод должен касаться зависимости величины ПЭК от химической структуры полимера.
Литература
1. Кирпичников, П.А. Химия и технология синтетического каучука /П.А. Кирпичников, Л.А. Аверко-Антонович, Ю.О. Аверко-Антонович. – Л.: Химия, 1970. – 528с.
2. Догадкин, Б. А. Химия эластомеров / Б.А.Догадкин, А.А. Донцов, В.А.Шершнев. – М.: Химия, 1981. – 376 с.
3. Практикум по высокомолекулярным соединениям. – М.: Химия, 1985. – 224 с.
Лабораторная работа № 5
ВЛИЯНИЕ ПРИРОДЫРАСТВОРИТЕЛЯ
НА СКОРОСТЬ НАБУХАНИЯ СЕТЧАТОГО ПОЛИМЕРА
Цель работы. Измерение скорости и определение постоянной набухания сетчатого эластомера в различных растворителях.
Установление влияния природы растворителя на величину и скорость набухания сетчатого эластомера.
Краткая теория
Установление склонности к набуханию имеет большое значение для оценки качества некоторых видов каучуков, применяемых для изготовления резиновых изделий, работающих в среде растворителей.
Первой стадией растворения любого полимера является его
набухание.
Различают ограниченное и неограниченное набухание.
Полимеры пространственно-сетчатого строения не могут полностью растворяться из-за наличия поперечных химических связей. Они способны лишь ограниченно набухать, образуя гели. Увеличение количества поперечных связей приводит к уменьшению способности полимера поглощать низкомолекулярную жидкость; при наличии густой пространственной сетки полимер полностью теряет способность набухать. Это можно проиллюстрировать рядом примеров. Так, при увеличении содержания серы в полимере способность вулканизатов к набуханию непрерывно уменьшается. Эбонит (вулканизат, содержащий около 32 % серы) совершенно не набухает. В данной работе, как впрочем, и в большинстве работ этого пособия, студентам выдаются образцы резин на основе различных по химическому строению каучуков.
Ограниченным набуханием называется процесс взаимодействия полимеров с низкомолекулярными жидкостями, ограниченный только стадией их поглощения полимером; самопроизвольного растворения полимера не происходит. При этом образуются две сосуществующие фазы. Одна фаза представляет собой раствор низкомолекулярной жидкости в полимере, другая является чистой низкомолекулярной жидкостью (если полимер совсем не растворяется) или разбавленным раствором полимера в низкомолекулярной жидкости. Эти фазы разделены ясно видимой поверхностью раздела и находятся в равновесии.
Для линейных полимеров этот процесс аналогичен ограниченному смешению жидкостей: при определенных условиях (температуре, концентрации компонентов) набухание ограниченно, но при соответствующем изменении условий оно может перейти в неограниченное растворение. Одним из таких условий является повышение температуры, способствующее разрушению физических связей между звеньями цепей.
Главным условием образования гомогенной, термодинамически устойчивой системы является степень сродства между полимером и растворителем. А она, в свою очередь, зависит от природы, как самого полимера, так и растворителя.
Если звенья цепей и молекулы растворителя близки по полярности, то энергия взаимодействия между однородными и разнородными молекулами примерно одинакова – происходит набухание (неограниченное или ограниченное). Если звенья цепи полимера и молекулы растворителя сильно различаются по полярности, то набухание происходит небольшое и растворения не наблюдается.
Неполярные полимеры (полиизопрен, полибутадиен) неограниченно смешиваются с предельными углеводородами (гексан) и не взаимодействуют с сильнополярными жидкостями (водой, спиртом). Полярные полимеры (целлюлоза, поливиниловый спирт) совершенно не взаимодействуют с углеводородами и хорошо набухают в полярных жидкостях.
Склонность полимера к растворению увеличивается с ростом гибкости его цепи. Увеличение температуры способствует увеличению гибкости цепей, что в свою очередь, облегчает отделение макромолекул друг от друга и ускоряет скорость их диффузии в растворитель. Поэтому полимеры с гибкими цепями, как правило, неограниченно набухают, т.е. растворяются. Большой гибкостью обладают полимеры с низким значением потенциальногобарьера вращения, не имеющие громоздких боковых разветвлений, полярных заместителей. Все эти факторы ведут, в конечном итоге, к уменьшению сил внутри- и межмолекулярного взаимодействия и повышению скорости набухания. С увеличением молекулярной массы полимера возрастает энергия взаимодействия между цепями в полимергомологическом ряду, следовательно, способность к растворению в одном и том же растворителе будет понижаться.
При рассмотрении влияния исходного фазового состояния полимера необходимо отметить, чтокристаллические полимеры растворяются значительно хуже, чем аморфные. Это объясняется наличием большого межмолекулярного взаимодействия из-за дальнего порядка расположения молекул. В этом случае для отрыва цепей друг от друга необходимо одновременно нарушить большое число физических связей, что требует значительной затраты энергии. Поэтому при комнатных температурах кристаллические полимеры, как правило, не растворяются даже в жидкостях, сходных по полярности.
Процесс растворения полимера в растворителе состоит из ряда последовательных стадий. На первой, молекулы растворителя, из-за значительно меньших размеров по сравнению с макромолекулами, проникают вглубь образца полимера в первую очередь в наименее плотно упакованные области поверхностных слоев. При этом молекулы растворителя вступают в физическое взаимодействие со звеньями макромолекул (идет сольватация). Визуально это проявляется в виде набухания полимера, так как образование сольватной «шубы» на макромолекулах из молекул растворителя раздвигает их и увеличивает объем. Увеличение расстояния между звеньями макромолекул приводит в конечном итоге к полному разрушению межмолекулярных физических связей. По этой причине макромолекулы полимера, не связанные с другими макромолекулами физическими связями, получают возможность диффундировать вглубь объема растворителя. Когда число таких макромолекул становится большим, это проявляется в виде уменьшения ранее достигнутой максимальной степени набухания. С этого момента можно уже с уверенностью заявлять, что стадия набухания завершилась и началась стадия растворения. Понятно, что полимеры сетчатого строения могут только ограниченно набухать в растворителях.
С практической точки зрения очень важно знать способность сшитых полимеров к набуханию в различных жидких и парообразных средах. Эта способность оценивается по степени набухания, которая выражается количеством поглощенной полимером жидкости (или ее пара), отнесенным к единице массы или объема полимера.
Состояние набухания характеризуют степенью набухания, которую определяют как количество поглощенной полимером жидкости, отнесенной к единице массы или объема полимера:
 ,
,
где m 0, V 0 – масса и объем исходного полимера;
m 1, V 1 – масса и объем набухшего полимера.
На рис. 18 приведена типичная зависимость степени ограниченного набухания полимера от времени.

Рис. 18. Типичная зависимость степени набухания от времени
Максимальная или равновесная степень набухания (q max)
определяется природой полимера и растворителя (сродством между ними), и густотой пространственной сетки полимера (при ее наличии).
Скорость набухания полимера лимитируется скоростью взаимной диффузии компонентов системы и для полимеров, находящихся в исходном высокоэластическом состоянии, обычно удовлетворительно описывается кинетическим уравнением первого порядка:
 , (16)
, (16)
где k – постоянная набухания;
q ¥ – максимальная (равновесная) степень набухания;
q – степень набухания в наблюдаемый момент времени.
После интегрирования уравнения (16) получим:
 . (17)
. (17)
По тангенсу угла наклона прямолинейной зависимости  от времени можно определить постоянную набухания k.
от времени можно определить постоянную набухания k.
Методика эксперимента
Реактивы, приборы и образцы: серный вулканизат каучука СКН–40, CCl4, C2H4Cl2, дилатометры, секундомер.
Скорость набухания определяют объемным методом, используя дилатометры.
Две небольшие пластинки резины (по 0,1–0,2 г) взвешивают на аналитических весах и помещают в дилатометры, один из которых заполняют CCl4, а другой – C2H4Cl2.
Набухание резины измеряют параллельно в двух растворителях, проводя замеры объема поглощенной низкомолекулярной жидкости через каждые 10 минут в течение 2 часов. Результаты эксперимента заносятся в таблицу 6.
Таблица 6
Экспериментально-расчетные данные процесса набухания
| t, с | D V | 
| 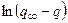
|
Строят графики зависимостей степени набухания (рис.19) и величины  от времени (рис.20) для двух растворителей и с учетом уравнения (17) находят постоянные набухания резины в CCl4 и C2H4Cl2. q ¥ определяют через две недели набухания.
от времени (рис.20) для двух растворителей и с учетом уравнения (17) находят постоянные набухания резины в CCl4 и C2H4Cl2. q ¥ определяют через две недели набухания.
Обсуждение полученных результатов
В результате проведения эксперимента и расчетов студент получает численные значения q max, k для серного вулканизата СКН-40, набухшего в CCl4 и C2H4Cl2. В данном разделе он должен объяснить различия в полученных значениях, рассматривая, в первую очередь, такое важное понятие как степень термодинамического сродства между полимером и растворителем.
С этой целью требуется вначале сделать качественный вывод о полярности каучука СКН-40 и растворителей. Для этого необходимо начертить структурную формулу звена СКН-40 и структурные формулы CCl4 и C2H4Cl2. Затем можно подтвердить сделанные качественные заключения о степени сродства каучука с растворителями сравнением их параметров растворимости s. Данные по величинам s растворителей можно взять в таблице 4 работы 4.
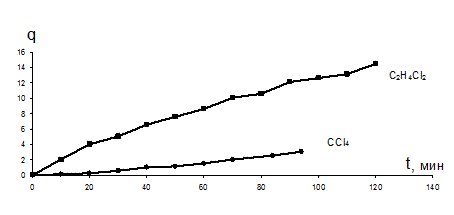
Рис.19. Зависимость степени набухания q от времени t
для CCl4 и C2H4Cl2
Следует учесть, что кинетика набухания определяется не только структурой исследуемого полимера и типом растворителя, но и геометрической формой образца. По этой причине для сравнения степени набухания различных полимеров необходимо использовать образцы одинаковые по размерам и форме. Желательно объяснить данный факт. Не следует забывать и о влиянии физического и фазового состояний полимера на склонность к набуханию.
 Рис.20. График зависимости
Рис.20. График зависимости  от времени в различных растворителях
от времени в различных растворителях
Выводы
В данной работе необходимо сделать вывод о влиянии термодинамического сродства полимера и растворителя на скорость и максимальную степень набухания.
Литература
1.Кирпичников, П.А. Химия и технология синтетического каучука / П.А. Кирпичников, Л.А. Аверко-Антонович, Ю.О. Аверко-Антонович. – Л.: Химия, 1970. – 528с.
2. Практикум по высокомолекулярным соединениям. – М.: Химия, 1985. – 224 с.
Лабораторная работа № 6
Оценка параметров пространственной сетки сшитого полимера по степени
равновесного набухания
Цель работы. Исследование структуры и степени сшивания вулканизатов на основе различных по химической природе каучуков.
Краткая теория
При наличии в полимере межмолекулярных химических связей набухание не может быть неограниченным. При контакте с низкомолекулярным растворителем сетчатый полимер ограниченно набухает, и равновесная степень набухания определяется плотностью поперечных связей и качеством растворителя.
Флори и Ренер провели теоретическое рассмотрение процесса набухания полимера сетчатого строения. Оказалось, что набухание такого полимера происходит до тех пор, пока осмотическая сила растворителя, проникающего в фазу полимера, не уравновесится упругой силой полимерной сетки.
Условию равновесия (моменту равновесного набухания) соответствует состояние трехмерной сетки, описываемое уравнением Флори–Ренера:
 , (18)
, (18)
где V k – объемная доля полимера в набухшем образце;
V 1 – мольный объем растворителя;
fy – функциональность узла сшивания; для тетрагональной сетки равна 4.
m – параметр взаимодействия каучука с растворителем.
Мc – молекулярная масса отрезка цепи между узлами сетки;
ρ – плотность эластомера.
Из уравнения (18) следует:
 . (19)
. (19)
Методика эксперимента
Пробы и реактивы:исследуют 2–3 вулканизата каучука, завулканизованных с применением различного количества серы и различных типов вулканизующих систем. Набухание образцов изучают в подходящем растворителе, для которого параметр взаимодействия m растворитель–полимер близок к 0,5 (см. табл. 8).
Для каждого типа вулканизата подготавливают по два образца, желательно, чтобы один образец имел форму квадрата с размером стороны 3 мм, а другой – прямоугольника размером 2´3 мм. Образцы взвешивают на торсионных весах, вес образца m 0 определяют по разности весов чашки с образцом и пустой чашки.
Взвешенные образцы помещают в бюксы (по 2 параллельных образца в один бюкс), предварительно пронумеровав их. В каждый из бюксов добавляют по 8 мл растворителя. Бюксы закрывают крышками и вместе с образцами оставляют до следующего занятия.
Все бюксы устанавливают в шкафу на бумагу, где указаны фамилии студентов, № группы, дата проведения работы и тип растворителя. Шифр бюкса и вес образцов заносится в рабочую тетрадь. Через неделю, каждый из образцов поочередно, пинцетом вынимают из бюкса, обмакивают в эфир, промокают фильтровальной бумагой, замечают по секундомеру 30 секунд. По истечении этого времени образец взвешивают на торсионных весах и определяют вес набухшего образца mH.
Для расчета параметра MC пространственной сетки полимера по формуле (19) используют значение равновесного набухания.
Объемную долюисходного полимера в набухшем геле рассчитывают по формуле:
 . (20)
. (20)
Значения rК и rР определяют из таблицы 9. Зная МС , рассчитывают степень сшивания j резин, то есть среднее число отрезков между узлами пространственной сетки, приходящейся на 1 макромолекулу эластомера:
 , (21)
, (21)
где М0 – молекулярная масса эластомера до сшивания.
При этом предполагается, что вулканизация протекала без деструкции исходного полимера.
Полученные данные и результаты вычислений заносят в таблицу 7.
Таблица 7
Экспериментальные данные степени сшивания
| m 0 | m H | 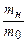
| 
| 
| 
| 
| 1– VK | ln(1– VК) | MС | j |
Сравнивая полученные значения MС и j, сделать выводы о степени структурирования изучаемых вулканизатов каучука.
Обсуждение результатов экспериментов
Данная работа проводится с образцами резин на основе полярного (СКН-40) и малополярного (СКИ-3) каучуков, подвергнутых равновесному набуханию каждый в двух растворителях, которые различаются по степени термодинамического сродства к набухаемому образцу.
Основная цель работы заключается в выяснении соотношения плотностей химической и физической сетки в резинах на основе полярного и неполярного каучуков.
Как правило, V k равна 0,25 или немного меньше в случае равновесного набухания среднесшитого сетчатого полимера в растворителе с близким значением параметра растворимости.
В этом случае, рассчитанная по формуле (19) величина М С будет отражать плотность химической сетки. В другом растворителе, с более далеким значением параметра растворителя по сравнению с параметром растворимости каучука, V к будет больше 0,25 и найденное значение М С будет отражать плотность сетки за счет химического сшивания и физического межмолекулярного взаимодействия. Рассчитав значения j по уравнению (21) для обоих случаев, можно в итоге определить доли химической и физической сетки в каждом из сетчатых эластомеров. Обсуждение результатов после получения этих данных должно касаться вопроса влияния химической природы каучука на уровень межмолекулярного физического взаимодействия в нем. Кроме того, нужно обратить внимание на наличие или отсутствие в испытываемом сетчатом эластомере активного наполнителя (технического углерода), способного образовывать с макромолекулами эластомера физические связи. При этом может образоваться такой вид НДС, как сажекаучуковая структура.
При обсуждении полученных результатов студент также должен обратить свое внимание на возможность сохранения в набухшем сетчатом эластомере кристаллических структур, если исходный эластомер способен кристаллизоваться.
Поскольку студентам при выполнении лабораторной работы выдаются сетчатые эластомеры разной степени сшивания, за счет неодинаковой дозировки сшивающего агента, то обязательно следует проанализировать влияние густоты химической сетки на уровень межмолекулярного физического взаимодействия.
Пример. В работе выдаются образцы на основе каучуков СКН-40 с 1 и 0,5 масс.ч и СКИ-3 с 1 и 0,5 масс.ч серы на 100 масс.ч каучука. Образцы вулканизатов СКИ-3 и СКН-40 подвергаются в течении не менее двух недель равновесному набуханию в растворителях, подобранных согласно значению m. После расчета М с и φ по данным равновесного набухания необходимо рассчитать доли химических и физических сшивок в вулканизатах СКН-40 и СКИ-3 и сделать соответствующие выводы.
Выводы
Кратко и лаконично перечисляются основные итоги раздела «Обсуждение результатов». По найденным значениям М с и φ и степени набухания в вулканизатах на основе каучуков СКИ-3 и СКН-40 делаются выводы о влиянии полярности каучуков на значения этих показателей.
Вопросы для самоподготовки и самоконтроля
1. Перечислите признаки истинных растворов полимеров.
2. Каковы особенности термодинамики растворения полимеров?
3. Дайте определение ограниченному и неограниченному набуханию полимеров.
4. Охарактеризуйте основные особенности процесса набухания полимеров.
5. Каково практическое значение растворов полимеров, какую роль они играют в технологических процессах синтеза и переработки полимеров?
Литература
1.Кирпичников, П.А. Химия и технология синтетического каучука / П.А. Кирпичников, Л.А. Аверко-Антонович, Ю.О. Аверко-Антонович. – Л.: Химия, 1970. – 528с.
2. Практикум по высокомолекулярным соединениям. – М.: Химия, 1985. – 224 с.
Таблица 8
Значения параметров взаимодействия полимер-растворитель при комнатной температуре
| Тип каучука | Растворитель | m | Плотность вулканизата (r к), г/см3 | |
| Натуральный Изопреновый СКИ-3 | Бензол | 0,421 | 0,91 0,92 | |
| Гексан | 0,480 | |||
| 1,1–дихлорэтан | 0,482 | |||
| Дихлорэтан | 0,494 | |||
| Гептан | 0,436 | |||
| CCl4 | 0,450 | |||
| Бутилкаучук | Циклогексан | 0,433 | 0,92 | |
| Гептан | 0,468 | |||
| Бензол | 0,50 | |||
| Декан | 0,519 | |||
| Этиленпропиленовый | Пентан | 0,440 | 0,86-0,87 | |
| Толуол | 0,490 | |||
| Этилбензол | 0,490 | |||
| Бензол | 0,580 | |||
| Силоксановый (диметилсилоксановый) | Пентан | 0,430 | 2,13 | |
| Толуол | 0,465 | |||
| Трихлорметан | 0,470 | |||
| Бензол | 0,520 | |||
| Бутадиен–нитрильный | СКН–18 | Этилбромид | 0,416 | 0,943 |
| Диоксан | 0,454 | |||
| Тетрахлорметан | 0,478 | |||
| СКН–26 | Этилбромид | 0,426 | 0,962 | |
| Диоксан | 0,455 | |||
| Тетрахлорметан | 0,686 | |||
| СКН–40 | Этилбромид | 0,489 | 0,986 | |
| Диоксан | 0,498 | |||
| Бутадиен-стирольный | СКС–30 | Дихлорметан | 0,474 | 0,944 |
| Циклогексан | 0,482 | |||
| Дибромметан | 0,497 | |||
| Диоксан | 0,538 | |||
| Хлоропреновый | Дихлорэтан | 0,533 | 1,21-1,25 |
Таблица 9
Параметр растворимости и плотность различных растворителей при комнатной температуре
1 (Дж/моль) – 0,2390 кал/моль
| Растворитель | Параметр растворимости s р | |
| (кал/см3)0,5 | (Дж/см3)0,5 | |
| Ацетон | 9,74 | 40,75 |
| Бензол | 9,22 | 38,58 |
| Бутанол | 10,77 | 45,06 |
| Гексан | 7,33 | 30,67 |
| Гептан | 7,48 | 31,34 |
| 1,2–дихлорэтан | 9,96 | 41,73 |
| Диэтиловый эфир | 7,74 | 32,43 |
| Октан | 7,60 | 31,84 |
| о. –ксилол | 9,03 | 37,84 |
| п. –ксилол | 9,03 | 37,84 |
| Пентан | 6,94 | 29,03 |
| Тетрахлорметан | 8,63 | 36,1 |
 Толуол Толуол
| 8,97 | 37,53 |
| Этанол | 12,87 | 53,84 |
| Этилацетат | 9,10 | 38,07 |
| Циклогексан | 8,25 | 34,52 |
Лабораторная работа № 7
ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОЙ МАССЫ
КАУЧУКА
Цель работы. Определение молекулярной массы полиизопрена вискозиметрическим методом на вискозиметре Убеллоде.
Краткая теория
Молекулярная масса – это одна из важнейших характеристик, определяющая физические, физико-химические и физико-механические свойства полимера, такие как прочность, твердость, температуростойкость. Существуют несколько методов определения молекулярной массы каучука, но наиболее оптимальным в лабораторных условиях является вискозиметрический метод.
Вискозиметрический метод. Характерной осо