Современные прикладные и фундаментальные науки в своих исследованиях нуждаются в высокочувствительных, быстрых и экономных методах анализа. Этого же требуют промышленные процессы, особенно биотехнологического профиля, где необходим точный техно-химический контроль.
Наряду с усовершенствованием различных физико-химических методов в последние годы разрабатываются и находят широкое применение те из них, где при анализе используются в качестве реагентов ферменты и другие биологические агенты для обнаружения разнообразных веществ.
Известно, что ферменты — это биологические катализаторы, обла-
дающие высокой специфичностью и ярко выраженной способностью избирательно катализировать многие химические превращения как в живой клетке, так и вне организма. Эти свойства ферментов давно привлекали внимание исследователей, в том числе аналитиков, но практическому их применению, например для аналитических целей, препятствовали прежде всего малая доступность чистых ферментов, неустойчивость во времени их растворов, препаратов при хранении и воздействии на них различных факторов (тепловых, химических), невозможность многократного использования одной порции фермента из-за сложности отделения его от других компонентов раствора, высокая стоимость очищенных препаратов. Однако выход из положения вскоре был найден, и появилась возможность применения каталитических свойств ферментов вне их связи с живым организмом и сохранения этой способности в течение длительного времени практически без изменения за счет перевода их в иммобилизованное (нерастворимое) состояние. Достижения в этой области биохимии и энзимологии положили начало развитию нового направления аналитической химии — безреагентных методов анализа, основанных на использовании различных биохимических сенсоров.
Биосенсор представляет собой устройство, в котором чувствительный слой, содержащий биологический материал: ферменты, ткани, бактерии, дрожжи, антигены/антитела, липосомы, органеллы, рецепторы, ДНК, непосредственно реагирующий на присутствие определяемого компонента, генерирует сигнал, функционально связанный с концентрацией этого компонента. Конструктивно он состоит из двух преобразователей, или трансдыосеров, — биохимического и физического, находящихся в тесном контакте друг с другом. На рис. 27 приведена общая схема такого устройства.
Биохимический преобразователь, или биотрансдыосер, выполняет функцию биологического элемента распознавания, преобразуя определяемый компонент, а точнее, информацию о химических связях в физическое или химическое свойство или сигнал, а физический преобразователь это свойство фиксирует с помощью специальной аппаратуры. В данном случае реализуется принципиально новый способ получения данных о химическом составе раствора. Наличие в устройстве биоматериала с уникальными свойствами позволяет с высокой селективностью определять нужные соединения в сложной по составу смеси, не прибегая ни к каким дополнительным операциям, связанным с использованием других реагентов, с концентрированием и т. д. (отсюда и название — безреагентные методы анализа).
Существует большое разнообразие физических трансдыосеров: электрохимические, спектроскопические, термические, пьезоэлектрические, трансдьюсеры на поверхностных акустических волнах и т. п. На рис. 28 приведен перечень преобразователей, используемых в биосенсорах. В настоящее время наибольшее распространение получили электрохимические их виды. Одни из них генерируют потенциал на
специальном электроде, на поверхность которого нанесен слой биоматериала, другие генерируют электрический ток реакции продукта превращения определяемого вещества на поверхности электрода, вызванного биоматериалом. Другими словами, существуют потенцио- и амперометрические биосенсоры. Если физический преобразователь использует изменение светопоглощения в области биослоя, то такой биосенсор называется, например, оптоволоконным, поскольку измеряемый сигнал будет передаваться измерительному прибору по оптическому волокну. Соответствующий физический преобразователь по аналогии с электродом называют оптродом. По названию преобразователя можно сделать вывод о характере физического свойства, которое измеряется аппаратно, причем, как правило, при этом используется микропроцессорная техника (см. рис. 27), позволяющая сделать устройство достаточно компактным.
 Схема ферментативной реакции
Схема ферментативной реакции
Е + S*=sES— E + Р Е — фермент, S — субстрат, ES — промежуточный комплекс, Р — продукт (фиксируется физическим преобразователем)

|
| ИШ&*&: |
Рис. 27. Принципиальная схема биохимического сенсора:
1 — исследуемый раствор; 2 — корпус биосенсора; 3 — полупроницаемая мембрана (для механического удержания биослоя); 4 — слой биоматериала; 5 — физический
преобразователь (электрод, пьезокристалл, оптоволоконный материал и т. д.); 6 — усилитель сигнала; 7 — самописец (дисплей, цифровой или световой указатель)
Первое упоминание об аналитических устройствах на основе ферментов или ферментсодержащих материалов появилось сравнительно недавно, в 60-х гг. прошлого столетия. Холинэстеразу, включенную в крахмальный гель и нанесенную на полиуретановую пластинку, использовали для обнаружения фосфорорганических инсектицидов в воздухе. Этот фермент очень чувствителен к фосфорорганическим соединениям, легко ими ингибируется. После пропускания анализируемого воздуха через ферментный датчик измеряют остаточную активность холинэстеразы. По разнице между исходной ее активностью и
активностью после контакта с воздухом по градуировочному графику находят концентрацию этих токсичных соединений. В настоящее время иммобилизованная холииэстераза используется в автоматических датчиках в промышленном производстве инсектофунгицидов для постоянного контроля воздушной среды цехов. Затем в обиход вошло понятие «биосенсор», или «биочип». Это важное событие в науке. Здесь отражаются глубокие причины, связанные с так называемыми интеграционно-синтетическими процессами в науке, приводящими к появлению новых знаний. Функционально, таким образом, биосенсоры сопоставлены с датчиками живого организма — биорецепторами, способными преобразовывать все типы сигналов, поступающих из окружающей среды, в электрические.
Биослой (биологический элемент распознавания)
Целые организмы
Живые ткани
Клетки
Органеллы
Мембраны клеток
Ферменты (индивидуальные)
Препараты ферментов
(неочищенные)
Рецепторы
Антитела
Нуклеиновые кислоты
Физический преобразователь
Потенциометрические
Амперометрические
Кондуктометрические
Импедансометрические
Оптические (оптроды)
Акустические
Тепловые
Механические
у Электроды
Рис. 28. Перечень преобразователей, используемых в биосенсорах
Принцип работы биосенсора достаточно прост. Определяемое вещество диффундирует через полупроницаемую мембрану в тонкий слой биокатализатора, в котором и протекает ферментативная реакция по схеме, указанной на рис. 29. Поскольку в данном случае продукт этой реакции определяется с помощью электрода, на поверхности которого закреплен фермент, то такое устройство еще называют ферментным электродом. Таким образом, понятия «биосенсор» и «фер-
242
ментный электрод» выступают в данном случае как синонимы. Большинство ферментативных процессов взимосвязаны, т. е. продукт одной такой реакции является субстратом другой. Если трудно идентифицировать продукт, то берется другой фермент, который превратит его в легко определяемое вещество. С помощью таких сопряженных реакций можно даже увеличить чувствительность анализа.

|
| Схема ферментативной реакции |
П
I тип биосенсора
На катоде (физический трансдьюсер):
| 2Н2О |
| ■4ОН" |
О2 + 4е
Ферментативная реакция (биологический трансдьюсер):
| Глюкозоксидаза ( |
| Н2О |
| S(ox) Глюк кислота) |
S(red) + О2
(Глюкоза)
Н2О2
(Глюконовая

|
II тип биосенсора
На аноде: Н2О2— >О2 + 2Н+ + 2е
Рис. 29. Схема работы глюкозного биосенсора:
1 — исследуемый раствор; 2 — корпус биосенсора; 3 — внешняя мембрана;
4 — слой глюкозоксидазы; 5 — внутренняя газопроницаемая мембрана;
6 — платиновый электрод (проволока) для восстановления кислорода;
7 — усилитель сигнала; 8 — самописец (дисплей, цифровой
или световой указатель и т. д.)
По-видимому, самым распространенным в настоящее время является амперометрический биосенсор на основе иммобилизованной глюкозоксидазы для определения сахара в жидкостях. В качестве физического трансдьюсера в нем использован так называемый электрод Кларка. В настоящее время для определения глюкозы создано наибольшее число различных биосенсоров, что связано с необходимостью
контроля за содержанием сахара в биологических жидкостях, например в крови, при диагностировании и лечении некоторых заболеваний, прежде всего диабета. Схема воздействия биосенсора на глюкозу в принципе типична и для других амперометрических его видов с аналогичным трансдыосером (см. рис. 29). Ток восстановления на платиновом катоде кислорода прямо пропорционален его концентрации. В присутствии субстрата (например, глюкозы в крови, взятой для анализа) ферментативная реакция понижает концентрацию О2. Таким образом, ток восстановления кислорода уменьшается пропорционально концентрации субстрата:
Глюкозоксидаза
Глюкоза + О2--------------------- ► Глюконовая кислота + Н2О2
Преимущество данного типа биосенсора, основанного на кислородном электроде Кларка, состоит прежде всего в его высокой селективности. Эта избирательность определяется особой специфичностью глюкозо-ксидазы и природой электрохимической реакции, в которой участвуют компоненты ферментативного процесса. В целом оксидазы являются высокоспецифичными по отношению к определяемым субстратам. Системы же на основе иебиологического преобразователя, напротив, не столь селективны, как этого бы хотелось, что обусловлено рядом причин. Тем не менее имеются ограничения и по применению данной конструкции биосенсора, обусловленные влиянием кислорода и других посторонних веществ, способных проникать через биослой (точнее, через мембрану), а потому задача совершенствования конструкций глюкозных биосенсоров представляется весьма актуальной.
Один из возможных путей такого усовершенствования заключается в следующем. Если изменить полярность включения электрода-трансдыосера в глюкозном биосенсоре на противоположную, т. е. платиновый катод Кларка сделать анодом, то при потенциале +0,6 В он становится совершенно невосприимчив к кислороду, но зато дает отклик на пероксид водорода, который при данном значении потенциала окисляется до воды. Эта чувствительность оказалась привлекательной, а поскольку Н2О2 образуется как продукт ферментативной реакции, по его содержанию можно сделать вывод о концентрации, например, глюкозы в различных объектах. Другой способ улучшения селективности биосенсоров и устранения помех от посторонних примесей состоит в использовании различных мембран — пленок, предотвращающих попадание этих веществ непосредственно на электрод-преобразователь. При этом внутренняя мембрана выполняет функцию защиты от примесей, а внешняя пропускает субстрат в биослой. Имеются и другие средства повышения избирательности физических преобразователей, в данном случае электродов. Например, с помощью специальных приемов, называемых химической модификацией, можно до такой степени изменить свойства поверхности электрода, что он будет «глухим» к большинству примесей и, напротив, чувствительным к компонентам ферментативной реакции.
Биосенсоры, основанные на кислородном электроде как физическом трансдьюсере, позволяют определять разнообразные субстраты ферментов: кроме глюкозы еще и лактаты, L -аминокислоты, салици-латы, оксалаты, пируваты, т. е. анионы соответствующих карбоновых кислот. В литературе описаны другие устройства подобного типа, ряд которых применяется на практике.
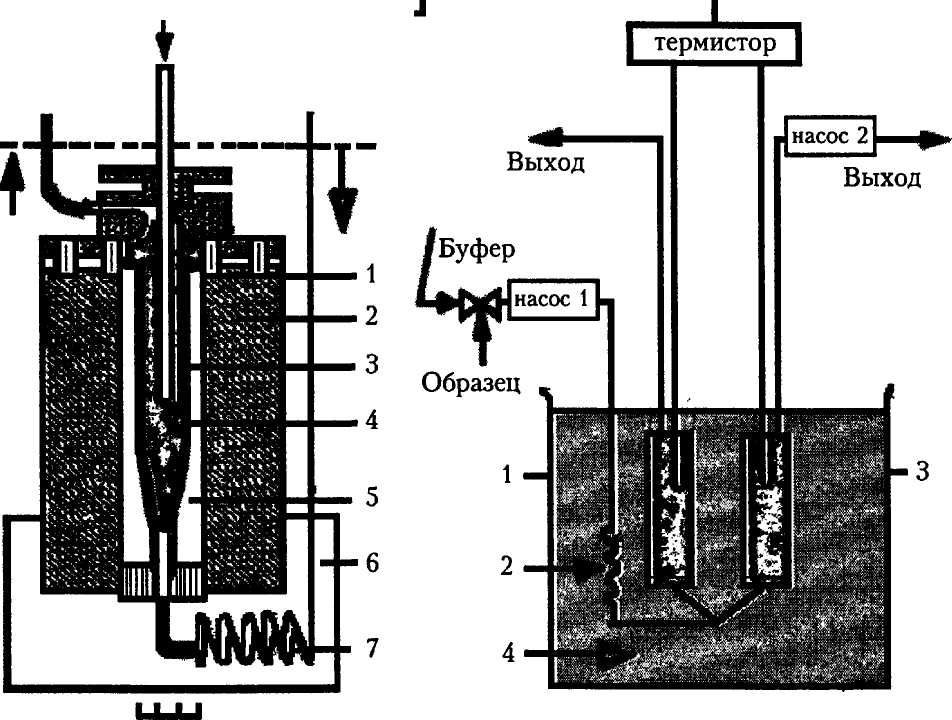
Для устранения влияния мутности и цвета исследуемых объектов на величину сигнала шведскими учеными был разработан микрокалориметрический датчик на основе иммобилизованных ферментов (рис. 30).
|
| | |
| самописец |
| L |
| термистор |— | самописец |
30 мм
а б
Рис. 30. Микрокалориметрический датчик для определения метаболитов: а — схема измерительного блока, где 1 — крепление колонки; 2 — металлический блок; 3 — термистор; 4 — микроколонка, заполненная иммобилизованным ферментом; 5 — внутренняя часть блока; 6 — водяная баня; 7 — теплообменник; б — общая схема установки, где 1 — измерительная колонка с ферментом; 2 — теплообменник; 3 — колонка сравнения с ферментом; 4 — водяная баня
С помощью биосенсоров можно решить и обратную задачу: при некоторой определенной концентрации субстрата оценить активность собственно фермента по величине измеряемого сигнала (потенциала, тока и т. д.). Последний зависит не только от концентрации субстрата, но и от каталитической активности биологического преобразователя, т. е. фермента. Такое использование биосенсоров позволяет изме-
рить активность большого числа ферментов, например, в крови. Так, оценка активности аспартатаминотрансферазы или креатинкипазы, связанных с сердечной деятельностью, позволяет в клинических условиях определить степень инфаркта миокарда. Измерение активности амилазы используется в педиатрии.
Многие ферменты дороги и быстро теряют свою активность, использование выполненных на их основе биосенсоров не может быть экономически целесообразным. Поэтому применение бактерий, микроорганизмов и биологических тканей различного происхождения более предпочтительно, поскольку в данном случае отпадает необходимость в предварительном получении и очистке биокатализаторов. К существенным недостаткам таких биосенсоров можно отнести низкую селективность вследствие того, что клетки живых организмов фактически являются источником самых разнообразных ферментов. Помимо этого время отклика данных устройств на основе тканей и микроорганизмов может быть достаточно большим, что также уменьшает их практическую ценность. Тем не менее в последние годы наблюдается повышенный интерес к разработке конструкций электродов, содержащих не сами ферменты в очищенном виде, а их первозданные источники — биологические материалы. Так, было установлено, что тканевые срезы в биосенсорах могут выполнять функцию источников каталитической активности. Например, создан тест на аскорбиновую кислоту, состоящий из упомянутого электрода Кларка и пластины кожуры огурца или тыквы, служащей источником аскорбиноксидазы. Активность фермента в такой природной матрице достаточна для проведения 50 — 80 определений аскорбиновой кислоты в различных объектах. Установлено, что пластины биоматериала могут храниться без потери активности в течение года в 50%-м глицерине.
Интерес представляют биосенсоры на основе иммобилизованных на мембране микроорганизмов, служащих элементом так называемого микробного сенсора. В качестве примера таких устройств можно назвать амперометрический сенсор, чувствительный к аммиаку (в сточных водах) на основе иммобилизованных нитрифицирующих бактерий и кислородного электрода Кларка. Он полезен при решении вопросов охраны окружающей среды, и, в частности, при контроле степени очистки промышленных стоков.
Можно отметить также использование биосенсоров на основе гид-ролаз — ферментов, являющихся катализаторами гидролитического расщепления субстратов. Эти устройства предназначаются, как правило, для эколого-аналитического контроля остаточных количеств пестицидов класса фосфорорганических соединений, а также для определения некоторых отравляющих веществ (ОВ). Действие таких биосенсоров может быть основано на следующих реакциях. Если при гидролизе какого-либо субстрата ферментом класса гидролаз образуется электрохимически активное соединение, то, следя за содержанием последнего, можно контролировать ферментативную реакцию так же,
как в предыдущих случаях. Однако в присутствии ингибиторов активность фермента уменьшается, что и обнаруживается по сигналу, регистрируемому электродом, причем чувствительность такова, что изменение определяется уже при действии очень малых количеств этих веществ — на уровне пико- и фемтограмм, т. е. 10"12 — 10~15 моль/л.
С учетом разнообразия ферментов, присутствующих и действующих в живом организме и являющихся потенциальными биологическими преобразователями, можно отметить, что существующее сегодня число конструкций биосенсоров может быть увеличено в десятки и даже сотни раз. Эти устройства получают распространение в биотехнологии. Хотя здесь и встречаются трудности, связанные с невысокой их термической устойчивостью, приводящей к дезактивации биослоя, есть основания полагать, что данный недостаток будет в скором времени преодолен. Так, полагают, что для увеличения срока службы биосенсоров в обозначенных выше условиях можно использовать ферменты, выделенные из термофильных бактерий и одноклеточных водорослей — микроорганизмов, устойчивых к действию высоких температур. Некоторые из этих устройств работают по принципу «да — нет», что вполне приемлемо, когда решается вопрос о присутствии ультрамалых количеств высокотоксичных веществ в объектах окружающей среды.
На очереди создание биосенсоров, заменяющих рецепторы живых организмов, что позволит создать искусственные органы обоняния и вкуса, а также применить указанные разработки для возможно более точной и информативной диагностики ряда заболеваний. Несомненно, что в ближайшем будущем в этой смежной области биологии и химии следует ожидать новых открытий.