Разработка метода полимеразной цепной реакции принципиально изменила ситуацию в исследованиях по направленному мутагенезу. Использование ПЦР для направленного мутагенеза основано на применении в качестве праймеров олигонуклеотидов, не полностью комплементарных матричной ДНК. Повышенные требования к комплементарности накладываются лишь на последний, 3’-концевой, нуклеотид праймера, но даже в случае 3’-концевой некомплементарности праймеры часто продолжают функционировать в системе ПЦР, хотя и с разной эффективностью. В то же время некоторая способность 17-нуклеотидного праймера инициировать ПЦР проявляется даже при наличии всего восьми нуклеотидов, комплементарных матрице, три из которых расположены на его 3’-конце. Таким образом, простейшим способом введения сайт-специфических мутаций в амплифицируемый фрагмент ДНК является использование праймеров, частично комплементарных матрице, т.е. содержащих необходимые мутантные нуклеотиды. Этот способ применяется для создания в амплифицируемом продукте новых сайтов рестрикции для последующего его клонирования. Такой подход удобен для встраивания амплифицируемого продукта в экспрессирующий вектор в одной открытой рамке считывания (ОРС) с инициирующим ATG-кодоном вектора. Действительно, как уже обсуждалось в главе 7, экспрессирующие векторы часто содержат 5’-концевую часть будущего рекомбинантного гена, включая регуляторные последовательности, промотор, ATG-кодон и иногда дополнительные кодоны нескольких последующих аминокислот. При конструировании таких векторов в последовательности, следующие за ATG-кодоном, вводят сайты рестрикции, по которым и встраивают фрагмент экспрессируемого гена, кодоны которого (для полноценной экспрессии гена) должны находиться в одной ОРС с ATG-кодоном вектора. Положение природных сайтов рестрикции в клонируемом гене редко отвечает требованиям ОРС вектора. Поэтому введение искусственных сайтов рестрикции в клонируемый фрагмент с помощью праймеров, не полностью комплементарных матрице, является хорошим решением проблемы.
Вырожденные праймеры, которые представляют собой сложную смесь олигонуклеотидов, содержащих многие точковые мутации, также используют для сканирования мутациями определенных участков ДНК. В таком классическом варианте постановки ПЦР кроме точковых мутаций можно легко получать делеции и вставки. Дальнейшим усовершенствованием метода направленного мутагенеза с помощью ПЦР явилась разработка подхода к получению гибридных генов с помощью перекрывающихся праймеров (рис. II.18). Этот метод позволяет не только целенаправленно получать точковые мутации, делеции и вставки, но и гибридные молекулы ДНК без применения ДНК-лигазы.
Для получения точковых мутаций используют пару праймеров, в которых изменен соответствующий нуклеотид или небольшая группа нуклеотидов (мутантный сайт обозначен на рис. II.18, 1 прямоугольниками внутри праймеров). При этом внутренние праймеры b и с комплементарны друг другу.
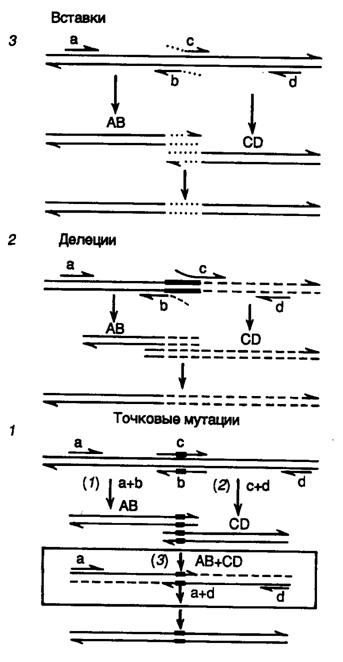
Рис. II.18. Использование ПЦР для получения мутаций
Получение точковых мутаций (1), делеций (2) и вставок (3): a и d – внешние праймеры, b и c – внутренние праймеры. AB и CD – фрагменты ДНК, образовавшиеся в результате ПЦР с использованием праймеров a и b, а также c и d соответственно. После гибридизации друг с другом объединяемых фрагментов ДНК сформировавшимися комплементарными последовательностями нуклеотидов одноцепочечные участки достраиваются ДНК-полимеразой в процессе ПЦР
В первых ПЦР в отдельных пробирках амплифицируют правую и левую части мутагенизируемого сегмента ДНК с использованием пар праймеров a + b и с + d, что приводит к образованию двух фрагментов ДНК, перекрывающихся на участках, которые содержат включенные праймеры (этапы 1 и 2). Фрагменты очищают от праймеров, смешивают друг с другом в эквимолярном соотношении и после цикла тепловой денатурации и ренатурации используют в качестве матрицы в другой ПЦР с внешними праймерами a и d (этап 3). На этом этапе в первом цикле ПЦР происходит достройка цепей перекрывающихся фрагментов ДНК (пунктирные линии на рис. II.12, 1), и образовавшийся фрагмент двухцепочечной ДНК, содержащий требуемую мутацию, далее служит матрицей для амплификации и по завершении ПЦР присутствует в реакционной смеси в препаративном количестве.
Тот же принцип объединения двух фрагментов ДНК, перекрывающихся за счет праймеров, используется при получении делеций и вставок. Для создания делеции (на рис. II.18, 2 обозначена прямоугольниками на цепях ДНК) берут внутренние праймеры b и с, 5’-концы которых комплементарны матрице по одну сторону делетируемой последовательности нуклеотидов, а 3’-концы – последовательности нуклеотидов, фланкирующей другой ее конец. Образующиеся при этом продукты ПЦР AB и СD перекрываются в точке делеции и далее используются, как и в предыдущем случае. При получении вставок (см. рис. II.18, 3) применяют внутренние праймеры b и с, комплементарные друг другу своими 5’-концевыми частями, которые соответствуют образуемой олигонуклеотидной вставке во фрагмент матричной ДНК. 3’-Концы этих праймеров комплементарны участкам ДНК-матрицы, непосредственно примыкающим к сайту, в который производится вставка олигонуклеотида.
С помощью метода ПЦР удается легко получать и множественные мутации в конкретных участках ДНК. В этом случае амплификацию мутагенизируемого сегмента ДНК производят в присутствии трех (вместо четырех) дезоксирибонуклеозидтрифосфатов, причем один из них вводят в реакционную смесь в высокой концентрации. Именно этот нуклеотид преимущественно включается в амплифицируемый фрагмент ДНК вместо недостающего нуклеотида, что сопровождается накоплением в ДНК-продукте множественных случайных мутаций в виде соответствующих замен нуклеотидов. В таких искусственных условиях мутации возникают за счет снижения точности функционирования ДНК-полимеразы.
Белковая инженерия
После рассмотрения способов получения сайт-специфических мутаций необходимо сделать лишь один шаг, чтобы оказаться лицом к лицу с бурно развивающимся направлением молекулярной генетики, называемым белковой инженерией. Действительно, разработка методов направленного мутагенеза дала возможность не только с высокой точностью модифицировать отдельные белки и изучать их структурно-функциональные взаимоотношения, но и конструировать новые белки, не существовавшие в природе. Впечатляющими результатами применения такого подхода являются гибридные белки, получаемые путем объединения фрагментов и функциональных доменов разных полипептидных цепей с использованием генно-инженерных методов.
Другое перспективное направление белковой инженерии – это конструирование биологически активных пептидов, обладающих фармакологической активностью.